2017年8月18日,美國總統(tǒng)簽署了"食品藥物管理局重新授權(quán)法”(FDARA),其中通過重新授權(quán)的還包括截止到2022年9月的《仿制藥用戶收費(fèi)案》 (GDUFA)。
今天,美國食品和藥物管理局微博發(fā)文稱"這是美國公共衛(wèi)生事業(yè)的一個(gè)勝利"。
非專利藥品使用者收費(fèi)重新授權(quán):公共衛(wèi)生的勝利
作者:凱瑟琳烏爾,邁克爾科普沙,
我們在2017年10月一日標(biāo)志著仿制藥計(jì)劃中的一個(gè)重要里程碑——仿制藥使用者費(fèi)用修正案(GDUFA)第一次重新授權(quán)的開始。這些來自行業(yè)的費(fèi)用為食品及藥物管理局提供了重要的資金,推動(dòng)了該機(jī)構(gòu)審查和批準(zhǔn)仿制藥申請的監(jiān)管工作。

凱瑟琳烏爾,歲,是食品及藥物管理局藥物評估和研究中心仿制藥辦公室主任
這不僅是食品及藥物管理局的里程碑,也是公共衛(wèi)生的勝利。增加消費(fèi)者獲得安全、高質(zhì)量和可負(fù)擔(dān)得起的仿制藥是食品及藥物管理局的首要任務(wù)。學(xué)名藥的價(jià)格通常只是名牌藥的一小部分,幾乎十分之九的處方都是用學(xué)名藥開的。在過去十年中,仿制藥為美國醫(yī)療保健系統(tǒng)節(jié)省了近1.7萬億美元。
雖然食品及藥物管理局在確定藥物定價(jià)方面沒有直接作用,但當(dāng)一種藥物的多個(gè)仿制藥版本獲得批準(zhǔn)時(shí),它會刺激競爭,并為消費(fèi)者提供負(fù)擔(dān)得起的選擇。
國會于2012年首次批準(zhǔn)向行業(yè)收取使用費(fèi),以幫助資助食品及藥物管理局的仿制藥項(xiàng)目,為期五年。除了傳統(tǒng)的國會預(yù)算撥款之外,在更長的一段時(shí)間內(nèi)獲得另一個(gè)資金來源,使我們能夠雇用更多的工作人員,更好地分配我們的審查活動(dòng)。因此,美國食品和藥物管理局批準(zhǔn)了創(chuàng)紀(jì)錄數(shù)量的仿制藥申請。
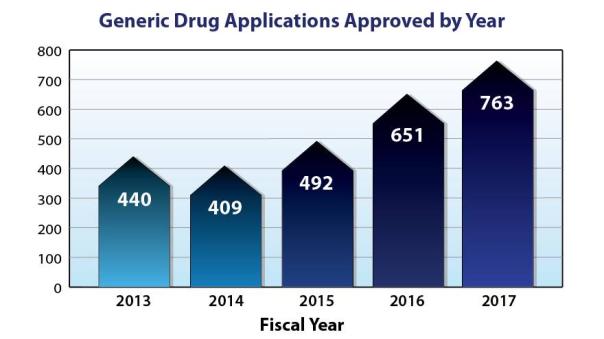
事實(shí)上,目前批準(zhǔn)的所有仿制藥的25%是在修正案的第一個(gè)五年期間批準(zhǔn)的。在修正案的最后兩年,美國食品和藥物管理局每年批準(zhǔn)的仿制藥比仿制藥項(xiàng)目歷史上任何一年都多100 . gdu fa的重新授權(quán)將有助于我們在這一成功的基礎(chǔ)上再接再厲。

邁克爾科普沙是美國食品和藥物管理局藥物評估和研究中心藥物質(zhì)量辦公室主任
使用者付費(fèi)支持專門的食品及藥物管理局工作人員審查仿制藥申請和檢查生產(chǎn)仿制藥的設(shè)施。用戶付費(fèi)為重要的信息技術(shù)基礎(chǔ)設(shè)施提供資金,幫助食品及藥物管理局管理不斷增加的工作量、提高效率并增加透明度。他們還資助重要的監(jiān)管研究,這些研究有助于澄清和改善作為仿制藥產(chǎn)品評估基礎(chǔ)的科學(xué)和臨床理解。
我們在修正案重新授權(quán)中同意的目標(biāo)和承諾支持公共衛(wèi)生。我們現(xiàn)在對公共衛(wèi)生優(yōu)先領(lǐng)域的申請有了更短的審查目標(biāo)。此外,這些目標(biāo)促進(jìn)了兩個(gè)主要目標(biāo):減少批準(zhǔn)仿制藥申請的時(shí)間和增加批準(zhǔn)的仿制藥數(shù)量。我們加強(qiáng)了與行業(yè)的溝通,以幫助確保該機(jī)構(gòu)收到完整、高質(zhì)量和科學(xué)合理的申請。另一個(gè)新功能是靈活的用戶收費(fèi)結(jié)構(gòu),以滿足小型企業(yè)的需求。這鼓勵(lì)了競爭,反過來可以降低消費(fèi)者的藥價(jià)。
開發(fā)復(fù)雜藥物產(chǎn)品的仿制藥——如吸入藥物或某些類型的注射藥物——具有獨(dú)特的挑戰(zhàn)100 .林業(yè)局將更早、更頻繁地會見申請人,以預(yù)測這些產(chǎn)品開發(fā)中可能出現(xiàn)的挑戰(zhàn)。
我們在修正案的經(jīng)驗(yàn)使我們能夠改進(jìn)審查流程,并實(shí)施與行業(yè)和消費(fèi)者溝通的最佳實(shí)踐100 . gdu fa的重新授權(quán)建立在頭五年的成功基礎(chǔ)上。我們期待在未來五年幫助美國公眾獲得更多負(fù)擔(dān)得起的高質(zhì)量仿制藥。
請?jiān)L問/仿制藥了解更多關(guān)于食品及藥物管理局仿制藥計(jì)劃的信息,并跟蹤重新授權(quán)的修正案的進(jìn)展情況。
凱瑟琳烏爾,歲,是食品及藥物管理局藥物評估和研究中心仿制藥辦公室主任
邁克爾科普沙是美國食品和藥物管理局藥物評估和研究中心藥物質(zhì)量辦公室主任
來自:FDA之聲
原標(biāo)題:美國總統(tǒng)重新授權(quán)《仿制藥用戶收費(fèi)案》 ,美國公共衛(wèi)生事業(yè)的一個(gè)勝利