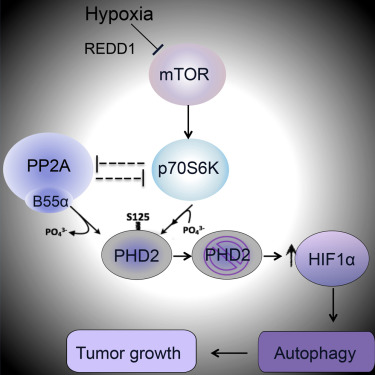
科學(xué)家最近發(fā)現(xiàn)了一種影響腫瘤生長的新機(jī)制。腫瘤內(nèi)的缺氧環(huán)境不僅能刺激增殖,還能影響蛋白質(zhì)PHD2,使其無法發(fā)揮“癌細(xì)胞殺手”的作用。研究人員發(fā)現(xiàn),要恢復(fù)PHD2的功能,可以阻斷PP2A/B55的作用,進(jìn)而延緩腫瘤的生長。相關(guān)研究成果發(fā)表在國際學(xué)術(shù)期刊《細(xì)胞報告》(Cell Reports)上。
癌癥預(yù)后不良往往與缺氧環(huán)境有關(guān),在缺氧環(huán)境中腫瘤細(xì)胞得不到氧氣供應(yīng)。蛋白質(zhì)PHD2是一種“缺氧受體”,其功能高度依賴于氧含量。研究小組重點研究了這種蛋白質(zhì)的磷酸化。
PHD2磷酸化后會變得更加活躍,促進(jìn)腫瘤缺氧區(qū)域的癌細(xì)胞死亡。但腫瘤過表達(dá)PP2A/B55,一種去除PHD2磷酸基團(tuán)的磷酸酶,導(dǎo)致PHD2部分失活,不能充分發(fā)揮“癌細(xì)胞殺手”的功能。
Massimiliano Mazzone教授說:“我們發(fā)現(xiàn)PHD2的磷酸化水平受到mTOR等信號通路的調(diào)節(jié)。這意味著我們的發(fā)現(xiàn)可能不僅適用于癌癥,也適用于其他疾病,如炎癥和代謝疾病。”
在人類癌癥樣本中,研究人員發(fā)現(xiàn)腫瘤中PP2A/B55的表達(dá)水平高于健康組織。Mazzone教授說:“這讓我們得出結(jié)論,PP2A/B55是癌癥治療的潛在靶點。因此,我們開始與一些合作伙伴研究針對PP2A/B55的潛在藥物。最終目標(biāo)是設(shè)計出能夠阻斷這種磷酸酶功能的分子,從而達(dá)到靶向治療癌癥的目的。”
這項研究不僅發(fā)現(xiàn)了癌癥治療的潛在靶點,還提供了一些新的生物標(biāo)志物:PHD2的磷酸化水平可能有助于了解腫瘤轉(zhuǎn)化的過程,并可以幫助選擇合適的治療方法。
Mazzone教授最后說:“為了完全理解這些過程,我們需要進(jìn)一步觀察腫瘤微環(huán)境和免疫系統(tǒng)。畢竟兩者都會影響腫瘤生長。”
本文來自生物谷。更多信息,請下載生物谷APP()