近日,北京北國(guó)生物科技有限公司(以下簡(jiǎn)稱“北國(guó)”)獲得中國(guó)食品藥品監(jiān)督管理局(CFDA)批準(zhǔn)頒發(fā)的“重組人肝細(xì)胞生長(zhǎng)因子裸質(zhì)粒注射液”三期臨床批件(批準(zhǔn)文號(hào):2017L04713),適應(yīng)癥為下肢動(dòng)脈缺血性疾病。
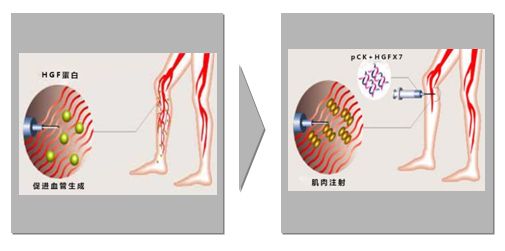
重組人肝細(xì)胞生長(zhǎng)因子裸質(zhì)粒注射液(以下簡(jiǎn)稱“本品”)是北京北國(guó)生物科技有限公司擁有自主知識(shí)產(chǎn)權(quán)的創(chuàng)新治療性生物制品,屬于基因治療裸質(zhì)粒藥物的研發(fā)。本品局部肌肉注射后,可通過骨骼肌細(xì)胞局部分泌兩種具有血管生成活性的肝細(xì)胞生長(zhǎng)因子異構(gòu)體,從而促進(jìn)血管生成,形成血管的“分子橋接”機(jī)制,增加血液供應(yīng),從而達(dá)到治療缺血性疾病的目的。該產(chǎn)品有望用于治療下肢動(dòng)脈缺血性疾病、糖尿病周圍神經(jīng)病變、心肌梗死等疾病。
下肢動(dòng)脈缺血性疾病屬于外周動(dòng)脈缺血性疾病,與冠狀動(dòng)脈缺血性疾病、糖尿病肢體動(dòng)脈閉塞性疾病一起,成為中老年人常見的外周血管閉塞性疾病。該類疾病治療療程長(zhǎng)、難度大、費(fèi)用高,致殘率和死亡率高,嚴(yán)重影響患者的健康和正常生活。目前,國(guó)內(nèi)外市場(chǎng)上還沒有針對(duì)下肢動(dòng)脈缺血性疾病的同類型產(chǎn)品。
達(dá)拉研發(fā)的重組人肝細(xì)胞生長(zhǎng)因子裸質(zhì)粒注射液創(chuàng)新藥物已在國(guó)內(nèi)完成I期和II期臨床試驗(yàn)。前期臨床試驗(yàn)結(jié)果初步驗(yàn)證了治療嚴(yán)重下肢缺血性疾病的安全性和有效性。根據(jù)CFDA相關(guān)法律法規(guī)的要求,創(chuàng)新藥物的研發(fā)需要通過三期臨床試驗(yàn),完成所有臨床研究獲得新藥證書后才能生產(chǎn)上市。達(dá)拉的創(chuàng)新藥物項(xiàng)目有望成為中國(guó)首個(gè)促進(jìn)血管生成的基因治療藥物。
本文來自生物谷。更多信息,請(qǐng)下載生物谷APP()