摘要
在藥品生產過程中,發生變化是非常正常的。即使在R&D能力相對較高的發達國家,每年控制一個品種在5-10個之間的變化也是很常見的,如果涉及到新產品、無菌產品、生物制品等。數量會更多。而在國內,目前對變化的控制還達不到國外的先進水平。如果控制執行不力,藥品質量安全的風險系數會大大增加。近年來,國內醫藥行業爆發的“藥害”事件,很多都是因為生產中的變更控制不力!
01
GMP系統~更改定義
在GMP體系中,變更~是指已批準上市的化學品的生產、質量控制和使用條件的變更,涉及來源、方法和控制條件。可以說,為了提高產品質量,生產出安全、有效、穩定的產品,所有的變更都可以視為變更。這些變化是主動的、有計劃的變化,可能影響藥品的安全性、有效性和質量可控性。變更的范圍包括原料、包裝材料、質量標準、檢驗方法、生產工藝、操作規程、工廠、設施、設備和儀器的變更。
02
GMP系統~變更分類
根據變更的性質、范圍和對產品質量的潛在影響,以及變更是否能影響注冊和變更時限等,有不同的分類方法。可以根據自己的實際情況選擇適合自己企業的分類方法。變更分類包括但不限于以下內容:
主要變更、一般變更和次要變更(目前企業使用最廣泛)
重大變更(需報藥監部門批準)是指將對產品質量產生重大影響的變更,主要包括:產品注冊標準的變更;更換內包裝材料;儲存條件、標簽和說明書的變更;關鍵合成路線、主要原料或溶劑、關鍵工藝參數和配方成分發生變化的;設備隨著運行方式和結構的變化、生產現場的變化等而變化。
一般變更(藥監部門備案)是指對產品內在質量(安全性、有效性)有潛在影響的變更,主要包括:生產和質量的主要設備、設施、儀器等關鍵部件的更換;生產合成工藝、質量標準和關鍵原輔材料供應商的變化;清洗方法的改變;包裝和標簽變更;GMP文件的變更等。
微小變更(無需申請批準或向藥監部門備案)是指不會影響產品安全性和有效性的變更。此類變更只需寫入年度質量報告即可。主要包括:設備設施附屬配件的更換;質量不變的原材料供應商的變更;中間生產場地變更等。
涉及注冊的變更和不涉及注冊的變更
在國內現行的藥品生產法律法規中,涉及變更的條款較多,如《藥品生產質量管理規范》,明確規定藥品生產企業應當嚴格按照注冊批準的生產工藝進行生產;規范中多次提到,生產工藝規程、操作規程或SOP藥品儲存條件要按照注冊標準執行。
055-79000甚至提到了很多地方變更登記的具體要求。例如,對已批準的新藥、已生產藥品、進口藥品的證明文件和附件中規定的項目進行變更的,應當提出補充申請;修訂藥品注冊標準,變更藥品處方中有藥用要求的輔料,變更影響藥品質量的生產工藝等。并提交補充申請;變更國內藥品生產企業名稱、變更國內藥品有效期、變更國內藥品生產企業內部藥品生產場所應當申報補充申請;藥品包裝標簽的變更應報補充申請等。
03
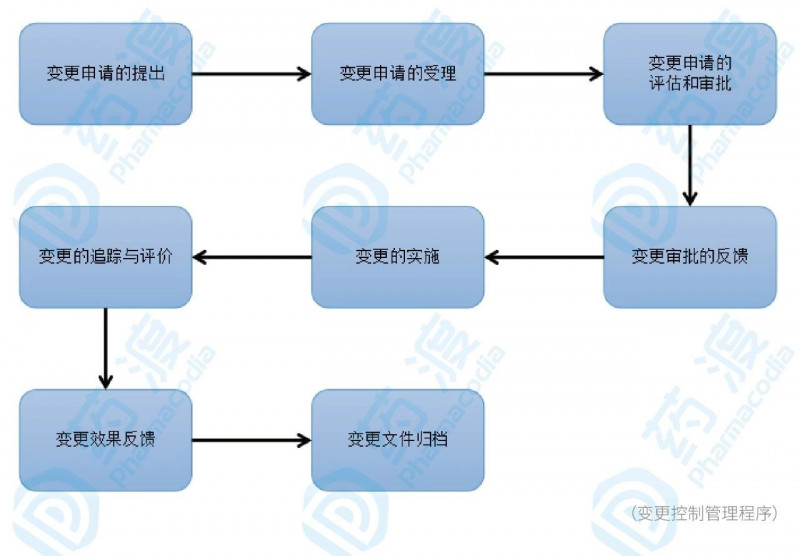
GMP系統~變更控制
在GMP系統中,變更控制是為了確保對已驗證的工藝、程序、文件、設備,
2.指定與此變更相關的所有部門進行審核。變更需報國家藥品監督管理局審批的,必須通知相關人員申報;
3.向主辦單位反饋各部門的意見;
4.監督變更過程中需要完成的所有工作是否按要求完全完成;
5.變化趨勢分析。
對已驗證系統的更改通常伴隨著不可預測的風險。因此,在變更的初始階段,應該進行詳細的評估,以確定變更是否必要。這種評價可以從以下幾個方面進行:
1.是藥監部門的要求嗎?
2.對員工安全有影響嗎?
3.符合規定嗎?
4.會提高產品質量還是生產效率?
04
總結/感受
在剛剛過去的2018年,國內醫藥行業發生了一系列疫苗事件,其中很大一部分是因為隱瞞了生產過程中的變化,造成了非常惡劣的影響。不僅企業自身承受了后果,對整個行業也產生了非常大的負面作用!藥品作為特殊商品,關系到生命,所以藥品全生命周期的質量控制自然是極其重要的!但是由于技術的進步和質量標準的不斷提高,生產上有相關的變化是非常正常和有意義的。GMP雖然追求穩定,但變革的本質不是挑戰穩定,相反是為了更長遠的穩定。我們藥學人要做的就是如何更好的控制變化,更好的服務于藥物的屬性!
全文數據:《藥品注冊管理辦法》;中國知網數據