1類化藥批準臨床概況
2018年6月,我國共有25個已申報臨床的一類化學新藥獲得臨床試驗批準文號,即將開始一期臨床試驗,其中15個為特批品種。抗腫瘤藥物依然是重頭戲——共16個,心血管系統2個,神經系統1個,肌肉骨骼系統1個,泌尿生殖系統疾病1個,呼吸系統1個。詳情如下:
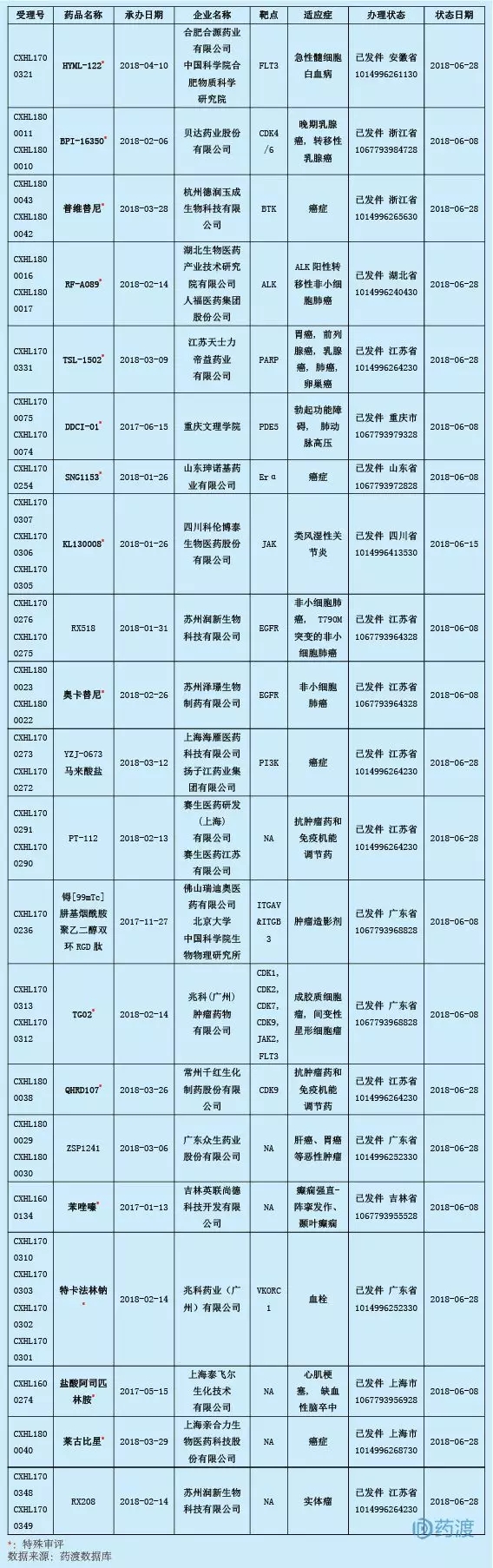
1. HYML-122
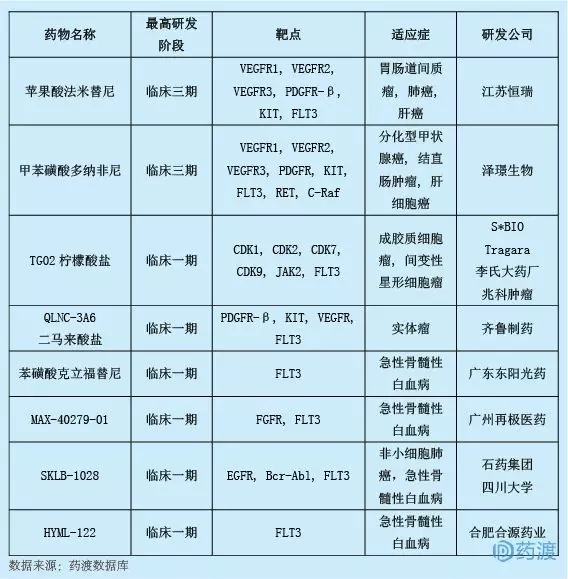
HYML-122由合肥和源藥業股份有限公司和中國科學院合肥物質科學研究所合作研發,是一種高選擇性的FLT3激酶抑制劑,擬用于治療急性髓系白血病。目前,FLT3激酶抑制劑的中國一類化學藥物有8個,具體如下:
2.BPI-16350
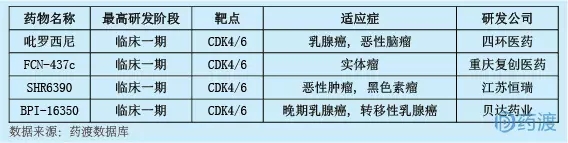
BPI-16350由貝達制藥有限公司研發,是一種細胞周期蛋白依賴激酶4/6 (CDK4/6)抑制劑,用于治療HR陽性/HER2陰性的絕經后晚期或轉移性乳腺癌。CDK4/6是調節細胞周期的關鍵因子,可以觸發細胞周期從生長期(G1期)向DNA復制期(S期)轉變。CDK4/6抑制劑阻斷細胞周期的G1期,從而抑制腫瘤細胞的增殖。目前,中國有四種1類CDK4/6抑制劑,均處于臨床I期,具體如下:
3.普維替尼
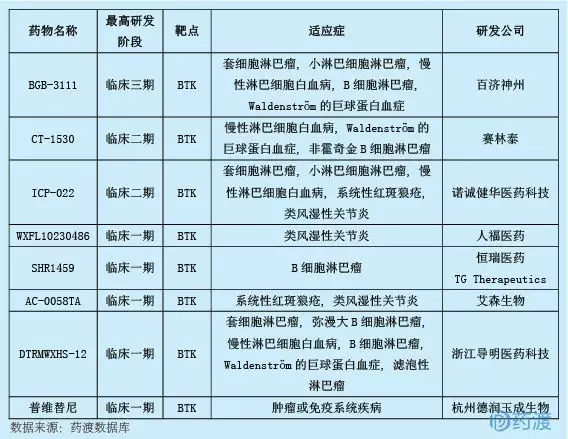
普替尼由杭州德潤宇成生物科技有限公司(蘇州韜略生物科技有限公司的子公司)研發,擬用于治療癌癥。據報道,該產品可能是一種BTK抑制劑。目前,我國BTK抑制劑的研發現狀如下:
4.RF-A089
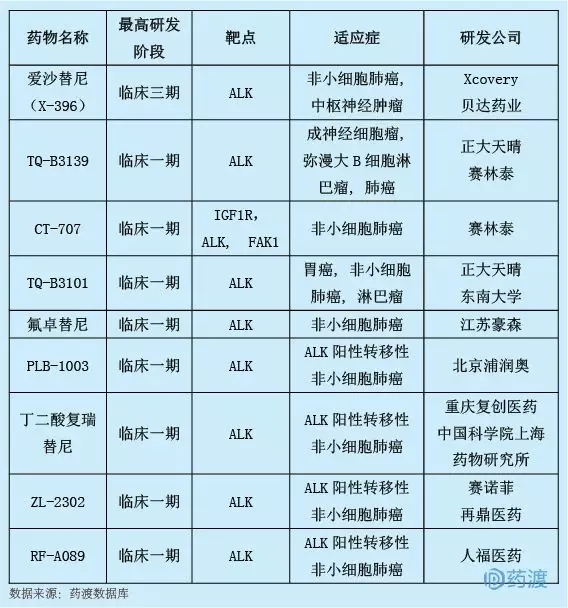
RF-A089是由人福藥業集團有限公司及其控股子公司湖北省生物醫藥工業技術研究所研發的新一代ALK抑制劑。它旨在用于治療ALK陽性的局部晚期或轉移性非小細胞肺癌。我國有9個一類新藥具有相同的靶點。詳情如下:
5.TSL-1502
TSL-1502是由天士力第一制藥(天士力集團控股公司)研發的具有自主知識產權的腺苷二磷酸聚合酶(PARP)抑制劑。其旨在用于治療卵巢癌、乳腺癌、前列腺癌、胃癌、肺癌和其他腫瘤疾病。目前國內一類新藥的PARP抑制劑有8種:
6.DDCI-01
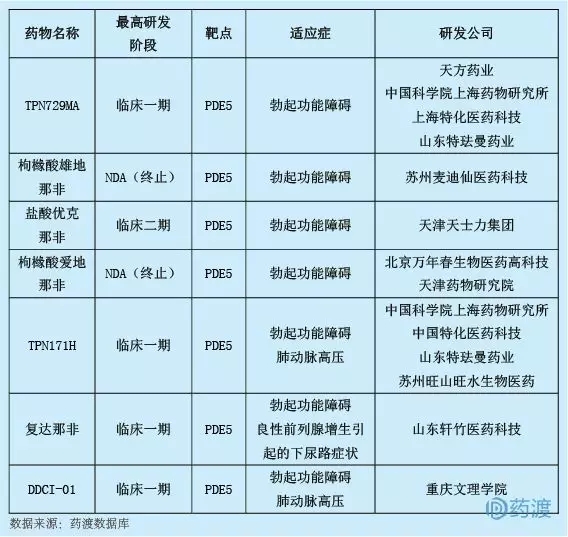
DDCI-01是由重慶文理學院研制的5型磷酸二酯酶(PDE5)抑制劑。用于治療肺動脈高壓和勃起功能障礙。目前,有7種PDE5抑制劑中國一類化學藥物,詳情如下:
7.SNG1153
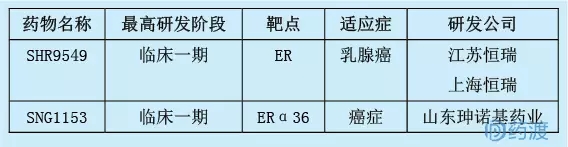
SNG1153是根據ACORADINE的結構進行修飾的小分子化合物,是山東申諾基制藥有限公司研發的雌激素受體ER-36調節劑,擬用于治療腫瘤。目前,中國有兩種針對雌激素受體的第一類化學藥物,詳情如下:
8.KL130008
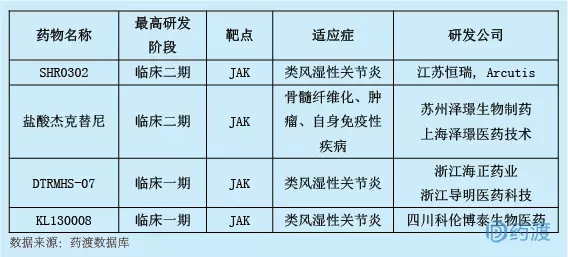
KL130008是四川科倫泰伯生物醫藥(科倫制藥子公司)公司研發的一種新型小分子JAK抑制劑,用于治療類風濕性關節炎。目前,共有四種JAK抑制劑中國第一類化學藥物,詳情如下:
9.RX-518
RX-518是一種表皮生長因子受體(EGFR)拮抗劑,由蘇州潤新生物和檢查點治療公司(Fortress Biotech的子公司)開發。在美國處于臨床I/II期,用于治療非小細胞肺癌。目前,EGFR抑制劑中國一類化學藥物共有48種,詳情如下:
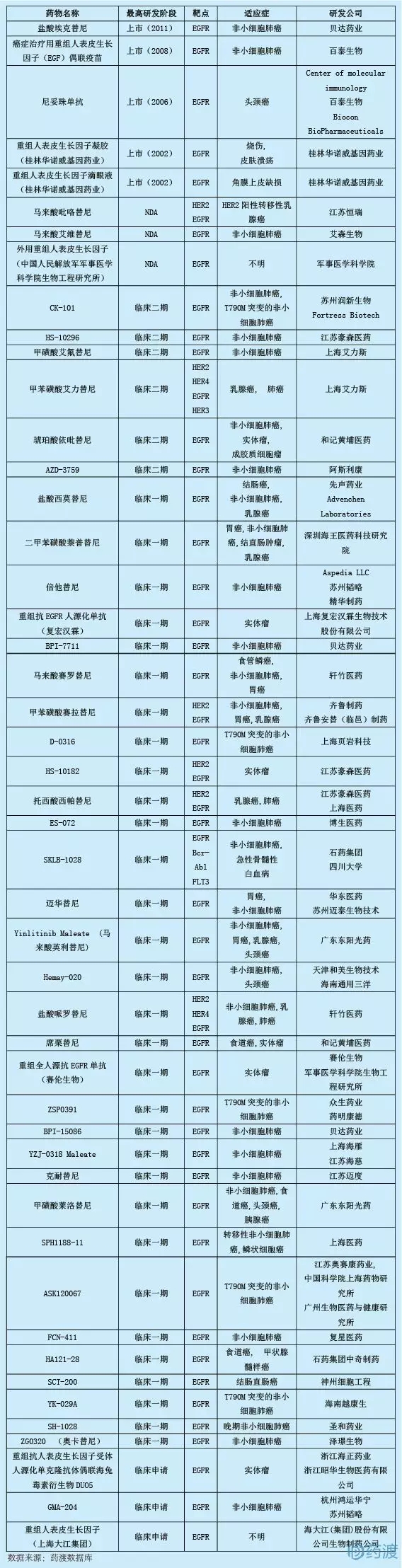
10.奧卡替尼
卡替尼可能是EGFR T790M抑制劑奧西替尼的氘代產物,用于治療非小細胞肺癌。本品由蘇州澤京生物制藥有限公司研制.目前,有8種EGFR抑制劑,中國一類,只針對T790突變。詳情如下:
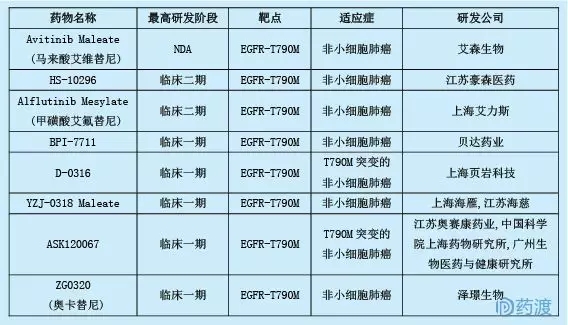
11.YZJ-0673馬來酸鹽
YZJ-0673馬來酸鹽為泛PI3K抑制劑,為口服小分子抗腫瘤藥物,由楊紫茳藥業研發平臺上海海燕自主研發。目前,共有八種PI3K抑制劑中國第一類化學藥物,詳情如下:
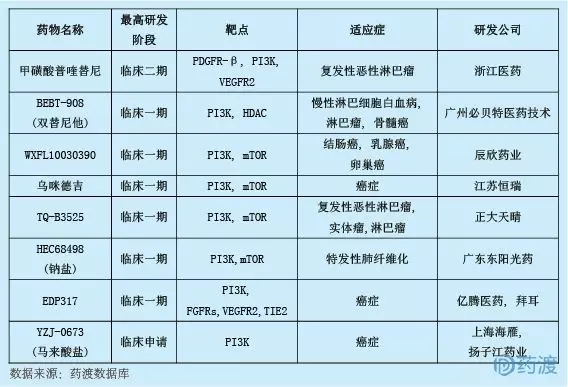
12.PT-112
PT-112是由Phosplatin Therapeutics開發的一種新的焦磷酸鉑試劑,旨在避免常規化療的毒性和耐藥機制。它會導致癌細胞死亡,從而釋放出可以再生的粒子
目前該藥在國際上正在進行治療晚期實體瘤和非小細胞肺癌的臨床I/II期試驗,該產品也在進行多發性骨髓瘤的臨床I期試驗。2018年2月,PT-112獲得美國FDA孤兒藥資格,用于治療多發性骨髓瘤。
2015年,該藥被授權給SciClone制藥。2018年2月,賽克隆制藥R&D(上海)有限公司向中國美國食品藥品監督管理局(化學藥物一類)提交了臨床試驗申請,并于2018年6月獲得了臨床試驗批準文件。目前,國內共有四種創新鉑類藥物,具體如下:
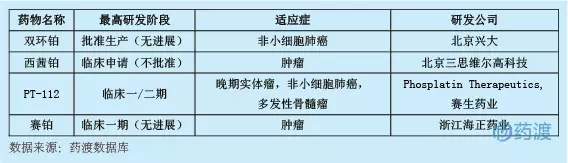
13.锝[99mTc]肼基煙酰胺聚乙二醇雙環RGD肽
锝[99mTc]肼基煙酰胺聚乙二醇雙環RGD肽是北京大學醫學部王凡教授研制的特異性腫瘤顯像劑。2014年,該成果以3000萬元成功轉讓給佛山瑞迪奧藥業有限公司。該藥物為整合素v3調節劑,由佛山市瑞迪奧制藥有限公司、北京大學和中國科學院生物物理研究所聯合申報的一類臨床應用。2018年6月,獲得臨床試驗批文。
本項目的優勢在于多肽與放射性核素螯合,多肽與放射性核素之間還連接有藥代動力學修飾分子,進一步增強結合親和力和腫瘤對藥物的攝取,對腫瘤達到更好的成像效果。因此,這些藥物可應用于各種原發性和轉移性腫瘤的影像學檢查,在腫瘤的早期診斷、臨床分期、個體化治療和療效評價方面具有廣闊的應用前景。項目學校擁有全部自主知識產權,并獲得多項國家專利。該藥是中國首個以整合素v3為靶點的一類化學藥物。
14.TG02 (檸檬酸鹽)
TG02及其枸櫞酸鹽最初由S*BIO公司研發,Tragara公司于2009年1月獲得了這種藥物的研發管理權。2015年11月,李氏藥業控股有限公司的子公司中國腫瘤焦點有限公司獲得Tragara授予的特許經營權,李氏藥業獲得在以下國家或地區開發和銷售TG02的獨家權利,包括中國大陸、香港、澳門、臺灣省、文萊、柬埔寨、東帝汶、印度尼西亞、老撾、馬來西亞、緬甸、菲律賓和新加坡。化合物TG02在中國的IND申報由李氏制藥公司的子公司趙可(廣州)腫瘤藥物有限公司提交。
TG02是一種以CDK9為主要抑制靶點的多激酶抑制劑,可同時抑制細胞周期蛋白依賴性激酶(CDK1/CDK2/CDK7/CDK9)、Janus激酶2 (JAK2)和Fms樣酪氨酸激酶3 (FLT-3)。目前,Tragara正在進行退行性星形細胞瘤和膠質母細胞瘤治療的臨床I/II期研究。Tagara還對多種晚期血液系統惡性腫瘤的治療進行了臨床I期研究,包括復發性或難治性急性和/或慢性淋巴細胞白血病、小淋巴細胞淋巴瘤、急性髓細胞白血病(AML)和多發性骨髓瘤(MM),但最近沒有取得研究進展。
15.QHRD107
目前國內另一個在研的CDK9抑制劑是常州洪倩生化制藥有限公司的QHRD107,其申報適應癥為急性髓系白血病(AML),這是國內申報的第二個CDK9抑制劑,也是洪倩生化制藥有限公司獲得的第一個一類新藥臨床批件
16.ZSP1241
ZSP1241是由眾生藥業股份有限公司和上海藥明康德新藥開發有限公司共同研發的具有明確作用機制和自主知識產權的創新藥物。主要用于治療肝癌、胃癌等惡性腫瘤。臨床前研究結果表明,ZSP1241在體內外均有較強的抗腫瘤作用,對多種肝癌和胃癌CDX或PDX模型均顯示出顯著的抗腫瘤作用,并與肝癌一線藥物索拉非尼有協同作用。GLP結果表明ZSP1241是安全的,具有較高的安全治療窗。據報道,成本產品可能是SMO抑制劑。目前國內又有一種SMO抑制劑在國內申報,即江蘇恒瑞申報的cicatrix (R&D代碼:SHR1539),已在國內進行實體瘤治療的臨床試驗(CTR20150231)。
17.苯唑嗪
苯扎嗪由吉林連贏尚德科技有限公司開發,旨在用于強直陣攣性癲癇的治療
18.特卡法林鈉
咖啡酸鈉是一種維生素K環氧化物還原酶復合物1 (VKORC1)拮抗劑。它是由海門匯聚藥業有限公司和趙可醫藥(廣州)有限公司共同研發的抗凝血藥物,但國內沒有相同的靶點。
19.鹽酸阿司匹林胺
鹽酸阿司匹林由上海泰菲爾生化科技有限公司研發,是一種用于治療缺血性中風和心肌梗死的藥物。
20.萊古比星
萊谷必興由上海親和生物醫藥科技有限公司研發,擬用于治療腫瘤。
21.RX208
RX208由蘇州潤鑫生物研發,擬用于實體腫瘤的治療。
1類生物藥批準臨床概況
2018年6月,我國共有12個一類生物藥獲批臨床試驗,即將開始一期臨床試驗,其中8個為特批品種。抗癌藥有八種,心血管系統一種,代謝系統一種,抗感染一種。詳情如下:
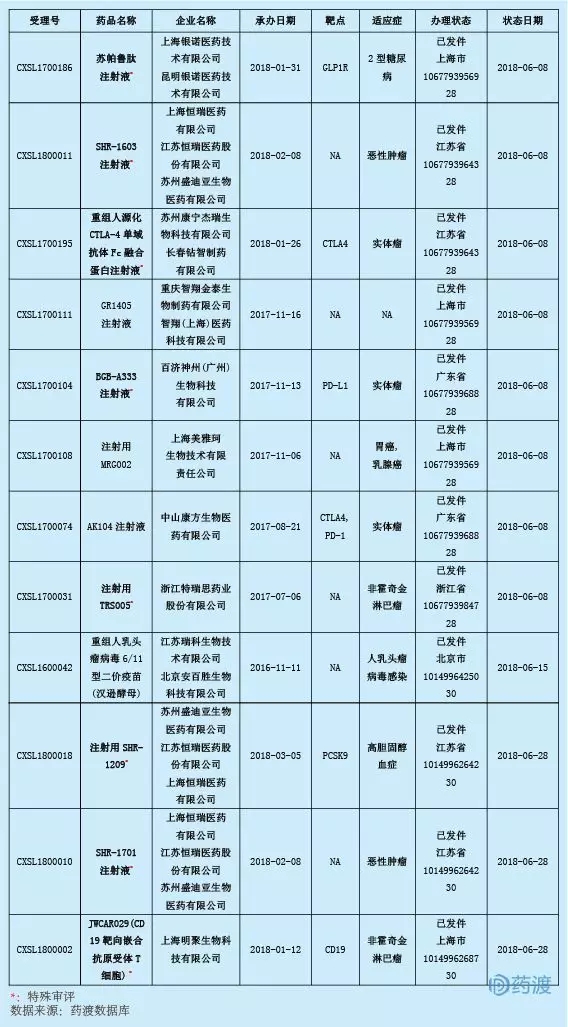
1.蘇帕魯肽
舒利迭注射液是胰高血糖素樣肽-1受體(GLP1R)激動劑,由銀諾醫療科技有限公司研發的長效降糖藥物,是采用基因工程重組蛋白技術生產的創新型生物制藥,擬用于治療二型糖尿病。長效GLP-1制劑方便,患者依從性更好,短效GLP-1制劑更具優勢。目前,以胰高血糖素樣肽-1受體(GLP1R)為靶點的中國一類藥物(生物藥和化學藥)有15個。詳情如下:
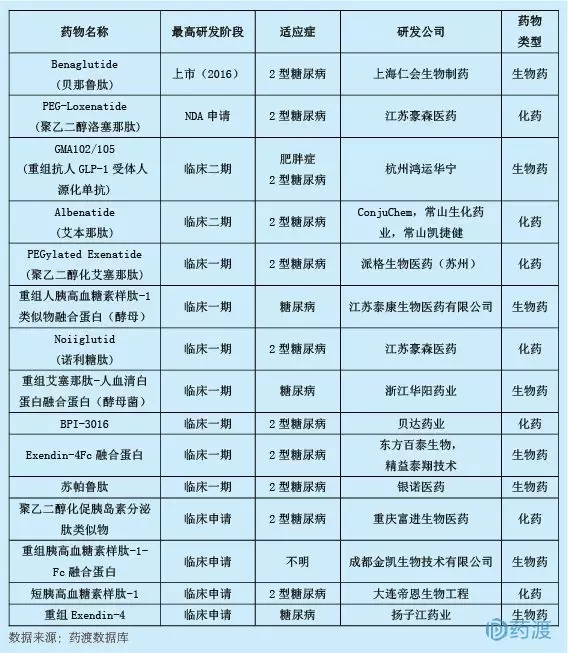
2.KN-044(重組人源化CTLA-4單域抗體Fc融合蛋白)
杰瑞研發的重組人源化CTLA-4單域抗體Fc融合蛋白注射液主要用于腫瘤的免疫治療。細胞毒性T淋巴細胞相關抗原4 (CTLA-4)在活化的CD4和CD8 T細胞表面表達,并在T細胞活化的初始階段起負調節作用。目前國內臨床應用一流的是康寧杰瑞的重組人源化PDL1/CTLA-4雙特異性單域抗體Fc融合蛋白(KN-046)和中山康方生物醫藥研發的靶向CTLA-4/PD-1的雙特異性抗體(AK-104)。截至2018年6月,KN-046和AK-104已在澳大利亞進行臨床試驗。
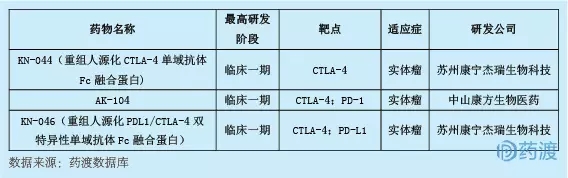
3.BGB-A333
BGB-A333是百濟神州研發的人源化單克隆抗體,針對程序性死亡配體1 (PD-L1)。目前,治療實體腫瘤的臨床I/II期試驗已經在澳大利亞開始。目前,有13個中國一類生物藥針對鈀L1,具體如下:
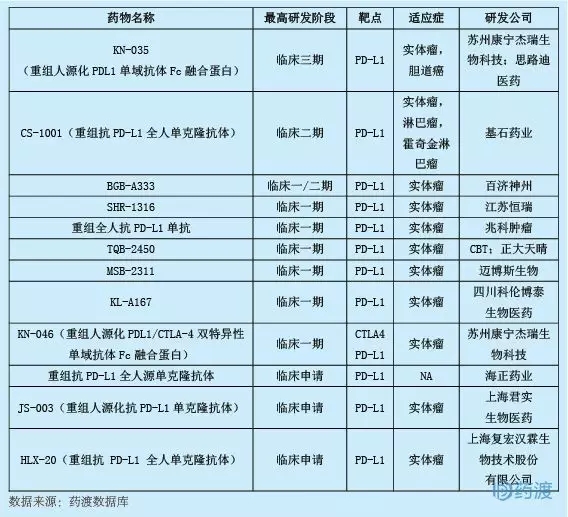
4.AK-104
AK-104是中山康方生物醫藥研發的雙特異性抗體,同時針對CTLA-4和PD-1。CTLA-4和PD-1是腫瘤浸潤性T細胞上共表達的免疫檢查點蛋白,AK104可以阻斷這兩種途徑。AK-104已經在澳大利亞開始臨床I期試驗,用于治療晚期實體腫瘤。由于PD-1抗體主要起到提高腫瘤微環境中效應T細胞的作用,而CTLA-4抗體主要激活外周淋巴結中的T細胞,兩者結合的效果值得期待。目前國內還沒有針對CTLA-4和PD-1的雙靶點藥物。針對CTLA-4的中國一類藥物和針對PD-1的14種中國一類生物藥物見KN-044。詳情如下:

5.MRG002
MRG002是上海美亞克生物科技有限公司研發的抗體偶聯藥物(ADC),通過高效的特異性抗原抗體反應,將抗腫瘤藥物直接攜帶至靶位,然后通過胞吞作用進入細胞內釋放毒素殺死腫瘤細胞。它兼顧了抗體的靶向性和化學藥物的致死性,因此成為腫瘤靶向研究的熱點。目前,我國有12種一類抗體結合藥物,具體如下:
6.SHR-1603
SHR-1603由恒瑞醫藥研發,用于治療惡性腫瘤,作用機制不明。
7.GR-1405
GR-1405由智翔(上海)醫藥科技有限公司及其子公司重慶智翔金泰生物制藥有限公司共同申報為第一類治療用生物制品。關于這個產品的詳細信息還沒有透露。
8.TRS005
TRS005是浙江特雷西制藥有限公司研發的抗體藥物偶聯物(ADC),擬用于非霍奇金淋巴瘤的治療。該品種已獲得國家“十二五”規劃“重大新藥創制”支持,并申請了3項中國專利和1項PCT國際專利。在其特殊的新藥審批制度支持下,成功獲得臨床批件
重組人乳頭瘤病毒6/11型雙價疫苗(漢遜酵母)由江蘇銳科生物和北京愛酶生物科學共同研發,擬用于預防宮頸癌。人乳頭瘤病毒誘發的疾病包括宮頸癌、陰道癌、陰戶癌、陰莖癌和肛門癌、某些類型的頭頸腫瘤、尖銳濕疣和復發性呼吸道乳頭狀瘤病。在全球范圍內,70%的浸潤性宮頸癌是由人乳頭瘤病毒16型(人乳頭瘤病毒-16)和人乳頭瘤病毒18型(人乳頭瘤病毒-18)引起的,其中人乳頭瘤病毒-16型誘發癌癥的潛力最大。人乳頭瘤病毒6型(人乳頭瘤病毒-6)和人乳頭瘤病毒11型(人乳頭瘤病毒-11)致癌風險低,但90%的尖銳濕疣和幾乎所有復發性呼吸道乳頭狀瘤病都是由這兩種基因型引起的。二價人乳頭瘤疫苗可預防70%的人乳頭瘤病毒感染,二價疫苗可預防91.2%的人乳頭瘤病毒感染。目前,中國有13種一類人乳頭瘤病毒疫苗。詳情如下:
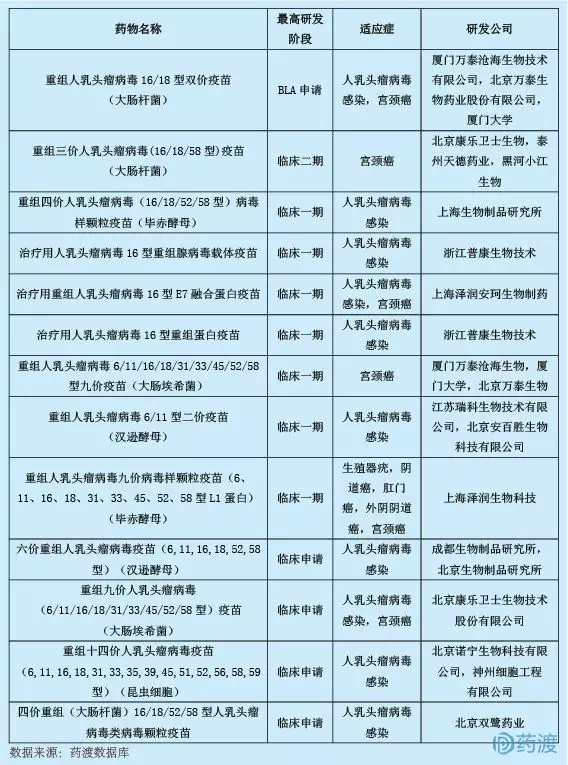
9.重組人乳頭瘤病毒6/11型二價疫苗(漢遜酵母)
SHR-1209由江蘇恒瑞及其全資公司蘇州圣迪雅生物醫藥共同研發,作為針對PCSK9的單克隆抗體,擬用于治療高膽固醇血癥。血液中的低密度脂蛋白膽固醇(LDL)可通過其受體(LDL-R)的特異性結合在肝臟中被清除,而人前蛋白轉化酶枯草桿菌蛋白酶9(PCSK9)可與低密度脂蛋白受體(LDL-R)結合,加速其降解,從而導致低密度脂蛋白膽固醇水平顯著升高。PCSK9抑制劑可以阻斷PCSK9與LDL-R的結合,使肝臟表面有更多的LDL-R清除LDL,達到降低體內膽固醇的作用。目前已有兩個PCSK9抑制劑Repatha (evolocumab)和Praluent (alirocumab)獲批上市,國內已申報5個一類新藥,其中CVI-LM001為口服小分子PCSK9抑制劑,其余為單克隆抗體。詳情如下:
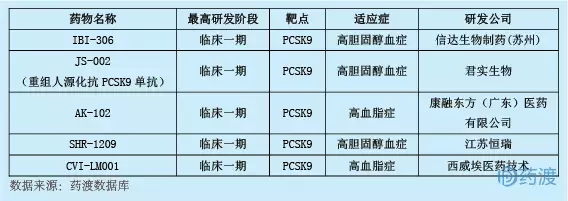
10.SHR-1209
SHR-1701注射液由江蘇恒瑞及其全資公司蘇州圣迪雅生物醫藥共同研發,擬用于晚期惡性腫瘤的治療。該公司沒有透露該藥物的目標信息。
11.SHR-1701
JWCAR029是基于美國Juno公司JCAR017,由無錫Juno(藥明康德集團與美國Juno公司于2016年共同創立)自主研發的CAR-T產品。2017年12月,通過關聯公司上海明聚生物科技有限公司提交IND申請,目前正在進行治療非霍奇金淋巴瘤的I期臨床試驗。2017年,隨著兩個CAR-T產品在血液腫瘤領域獲得FDA批準,相關審評政策在國內迅速實施,CAR-T的臨床應用迅速推廣。CAR-T療法作為生物藥物在中國有18項申請,具體如下:
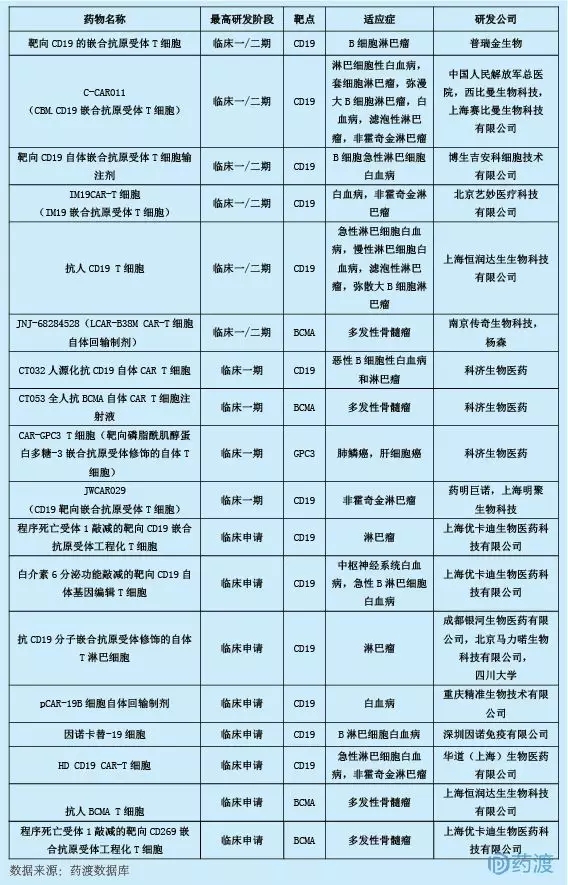
12.JWCAR029 (CD19靶向嵌合抗原受體T細胞)
2018年6月,CDE承擔了3項1類新藥的NDA申請,且全部集中在化學藥物。具體信息如下:
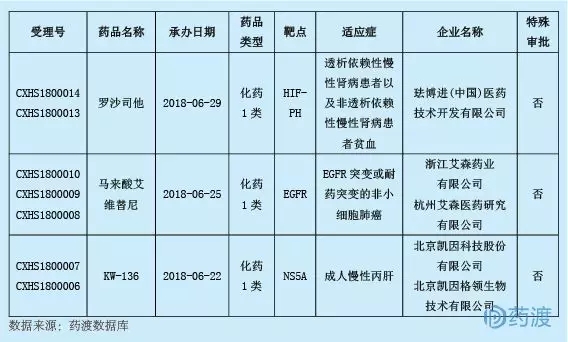
1類新藥NDA申請概況
Rosita (FG-4592)已經在中國提交了NDA申請,旨在用于治療透析依賴性慢性腎病(DD-CKD)患者和非透析依賴性慢性腎病(NDD-CKD)患者的貧血。國際上正在進行慢性腎臟病患者貧血的三期臨床研究,可用于降低血壓和膽固醇。
Rosita是缺氧誘導因子脯氨酰羥化酶(HIF-PH)的抑制劑,可以抑制HIF的泛素化降解,幫助機體產生更多的紅細胞。缺氧誘導因子(HIF)是一種蛋白質,能夠響應細胞環境中氧含量的變化,通過誘導紅細胞生成來滿足機體的需氧量。FG-4592通過人體的天然氧感應和反應系統幫助產生紅細胞,其機制類似于人體對高海拔(低氧含量)環境的自然反應。這是國內唯一的HIF-PH抑制劑,也是世界最高研發階段。被業界認為是首個全球研發的中國一類新藥。
Rosita最初由FibroGen(法博金)開發,2006年獲得亞洲、歐洲和南非Astaire的開發權。2013年,阿斯利康獲得了在美國、中國和除日本和歐洲以外的其他主要地區的開發權。
2014年4月,CDE承擔了Roxastat(化學藥物1.1類)的臨床試驗應用。
2015年8月,Roxastat首次獲批臨床試驗。
2017年9月,羅沙他的兩項關鍵III期臨床試驗結果公布:中國慢性腎臟病非透析患者III期研究顯示,羅沙他組患者血紅蛋白水平顯著升高;對中國慢性腎臟病透析患者的III期研究表明,羅沙司他優于現有的常用治療方法。因此,這兩個III期臨床試驗已經達到了主要有效終點。
2017年11月,CDE承擔了羅沙司他一類新藥上市申請,受理號為CXHS1700018、CXHS1700019、CXHS17000120。
2017年12月,羅莎被CDE列入優先審查對象。
2018年6月,CDE再次承擔了羅沙司他1類新藥上市申請,受理號分別為CXHS1800013和CXHS1800014。
1.羅沙司他
馬來酸阿伐替尼是艾森制藥自主研發的第三代EGFR靶向抑制劑,用于治療EGFR突變或耐藥突變的非小細胞肺癌。口服后,馬來酸依維替尼與包括T790M耐藥突變在內的EGFR突變株共價結合,抑制EGFR突變株的信號轉導,從而誘導細胞死亡,抑制EGFR突變腫瘤細胞的生長。由于該藥物對EGFR突變體具有選擇性,因此其毒性低于非選擇性EGFR抑制劑。
馬來酸阿伐替尼是中國第一個進入臨床研究的第三代EGFR抑制劑。獲得了國家“十二五”新藥創制的支持,也是中國美國食品藥品監督管理局和美國美國食品藥品監督管理局批準的國內首個進入臨床研究的創新藥物。馬來酸阿維替尼在中國的重要里程碑:
2013年8月,CDE承擔了馬來酸依維替尼的臨床試驗申請(化學醫學1.1)。
2014年9月,CDE發布了臨床試驗批準。
2014年9月,愛森制藥開始臨床I/II期試驗(NCT022274337)。
2017年2月,艾森藥業計劃進行臨床三期試驗(NCT03058094)。
2017年5月,愛森藥業啟動期臨床試驗(CTR20161018NCT03300115).
2018年6月,CDE承擔了馬來酸伊維替尼(化學藥一類)的上市申請,受理號分別為CXHS1800008、CXHS1800009、CXHS1800
Coblopasvir (KW-136)
Coblopasvir (KW-136)是一種NS5A抑制劑,它可以通過靶向非結構蛋白NS5A來抑制丙型肝炎病毒的復制。由北京開音科技有限公司開發,目前已提交在國內上市的申請。根據其已完成的臨床試驗(CTR20171654),它應與索非布韋聯合用于治療成人慢性丙型肝炎。其R&D里程碑:
2015年1月,CDE承擔了KW-136(化學醫學1.1)的臨床試驗應用。
2016年5月,CDE發布了臨床試驗批準。
2016年7月,凱恩科技啟動一期臨床試驗。
2017年3月,凱恩科技啟動了治療成人慢性丙型肝炎的II期臨床試驗(CTR20170073)。
2017年6月,凱恩科技啟動KW-136膠囊聯合索非布韋片治療成人慢性丙型肝炎的III期臨床試驗(CTR20171654)。
2018年6月,CDE承接了KW-136的上市申請,受理號分別為CXHS1800007和CXHS 180006。