1、類化藥臨床審批概況
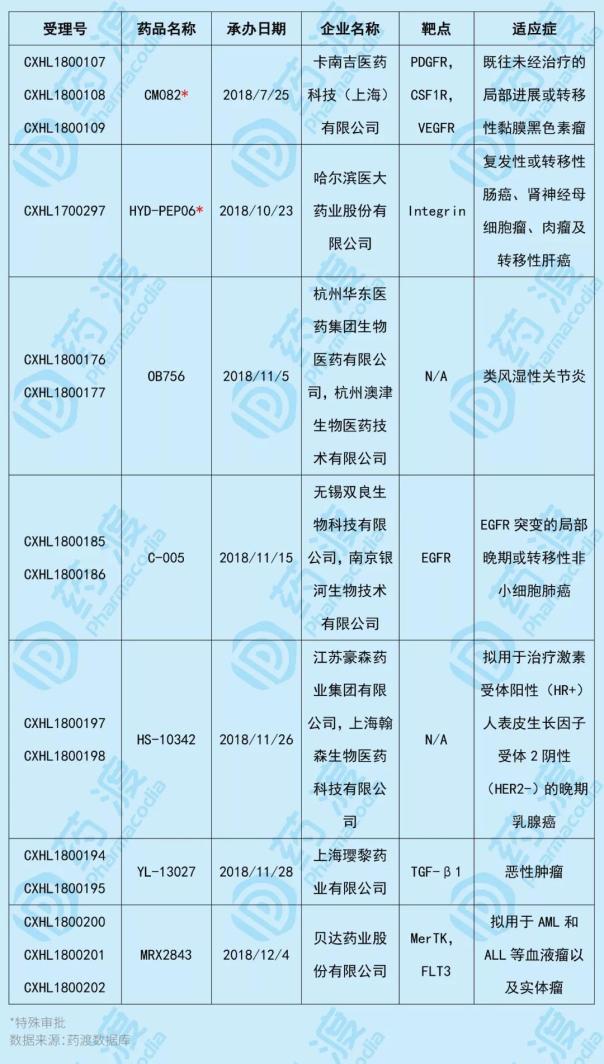
2019年1月,共有7個中國第一類化學藥品獲得國家醫藥產品監督管理局(NMPA)批準,其中2個為特殊批準品種。具體信息如下表所示:
1、CM082片
CM082片劑(Vorolanib)是一種針對VEGFR、PDGFR和CSF1R的多靶點受體酪氨酸激酶(RTKs)抑制劑,可抑制血管生成和腫瘤生長。該藥的研發目標是保留輝瑞舒尼替尼的藥效,并大幅降低其毒性。CM082片劑用于口服治療濕性年齡相關性黃斑變性(wAMD)、急性髓細胞白血病(AML)和各種晚期實體瘤,如非小細胞肺癌、胸腺瘤、胃癌、肝細胞癌、腎細胞癌、黑色素瘤、胰腺神經內分泌腫瘤等。
Vorolanib最初是由Tyrogenex (R&D代碼X-82)開發的。2009年,卡南吉醫藥獲得中國R&D授權(R&D代碼CM-082),春分科學獲得中國以外的R&D和商業化授權。2017年6月,卡南吉藥業成為貝達藥業的全資子公司。2018年6月,Equinox Science成為北大的全資子公司。截至目前,貝達藥業通過卡南吉擁有沃羅拉尼化合物(X-82)所有適應癥的國內權益,通過Equinox擁有海外權益。此外,貝達藥業的美國子公司Xcovery也在進行這種藥物的臨床研究。
2、HYD-PEP06
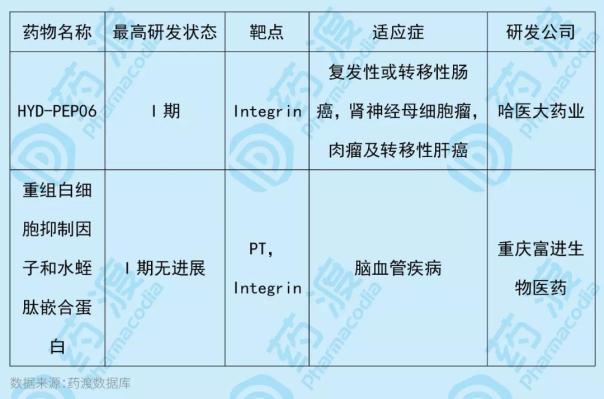
HYD-PEP06是固相化學合成的多肽類抗腫瘤藥物,含有30個氨基酸,其序列為RGDRGDMHSHRDFQPVLHLVALQSPLSGGM。多肽N端重復的Arg-Gly-Asp(RGD)基序可特異性結合腫瘤相關血管內皮細胞的整合素,抑制腫瘤血管生成、腫瘤增殖、營養吸收和代謝。HYD-PEP06是恩度的RGD修飾的仿生肽。通過合成方法解決了這種一線抗癌藥穩定性低、半衰期短、抗原性強的缺點。HYD-PEP06由哈醫大制藥有限公司研發,國內一類靶點相同的藥物如下表所示:
3、OB756片
OB756由杭州華東制藥集團生物醫藥有限公司和杭州金鰲生物醫藥科技有限公司研發,用于治療類風濕性關節炎。但該藥物的具體活性成分和作用靶點尚不清楚。
4、C-005片
C-005是一種新型的第三代EGFR抑制劑,用于治療EGFR突變的局部晚期或轉移性非小細胞肺癌。C-005由南京銀河生物和無錫梁爽共同開發,雙方各擁有50%的權益。與C-005靶點相同的中國一類新藥如下表所示:
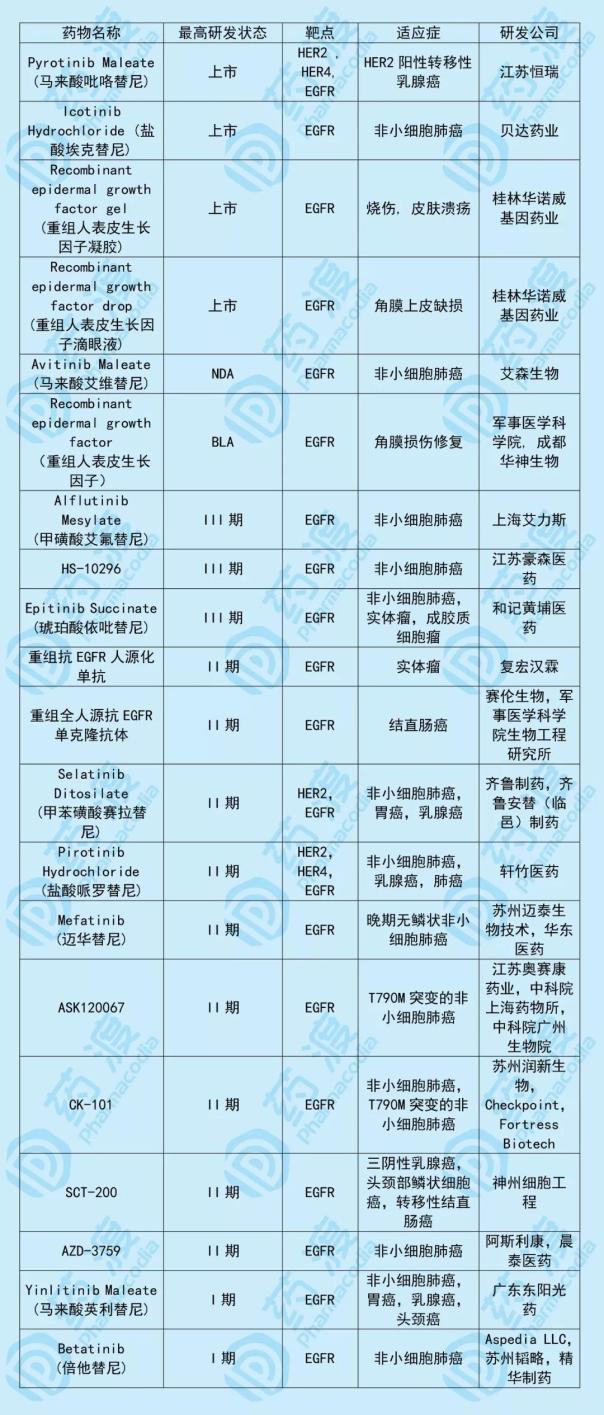
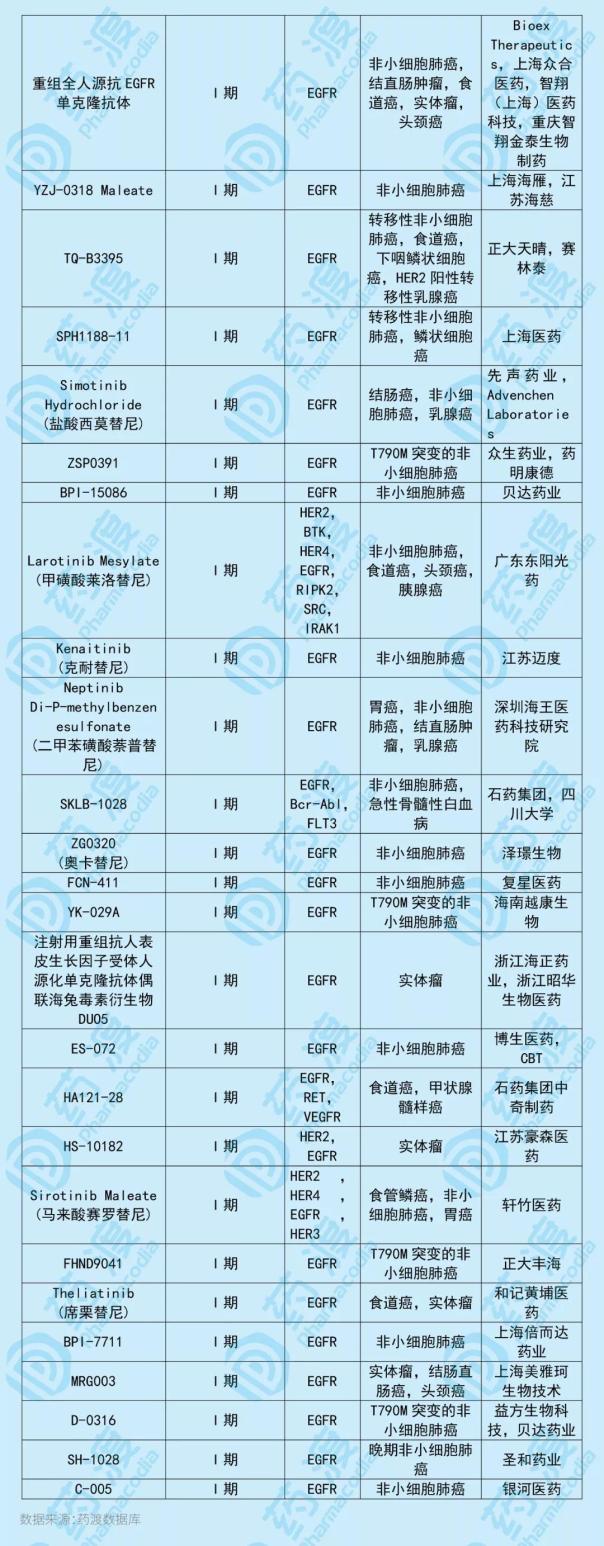
5、HS-10342片
HS-10342由江蘇豪森藥業集團有限公司及其子公司(上海漢森生物醫藥科技有限公司)研發,擬用于治療激素受體陽性(HR)和人類表皮生長因子受體2陰性(HER2-)的晚期乳腺癌。
6、YL-13027片
YL-13027是轉化生長因子1(TGF-1)的抑制劑,旨在用于治療惡性腫瘤。與YL-13027靶點相同的中國一類新藥如下表所示:
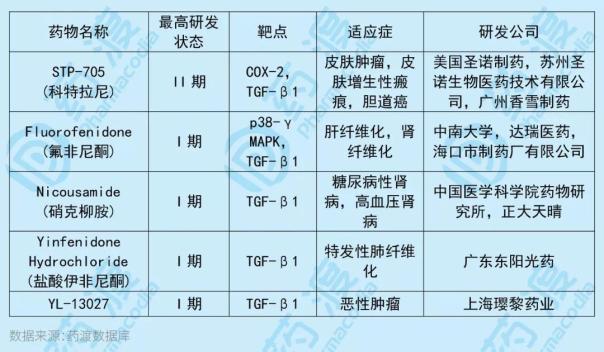
7、MRX2843片
MRX2843是一種雙重抑制劑,靶向Mer酪氨酸激酶(MerTK)和FMS樣酪氨酸激酶3(FLT3)。MerTK和FLT3在多種腫瘤中過表達,MRX2843可通過抑制腫瘤微環境中腫瘤細胞和先天免疫細胞上的MerTK和FLT3誘導腫瘤細胞凋亡。目前,該藥物正處于治療實體腫瘤的I期臨床研究和治療血液系統惡性腫瘤和血栓的臨床前試驗階段。
MRX-2843最初是由加州大學和北卡羅來納大學教堂山分校聯合開發的。Meryx在2013年7月被授權開發該藥物。2017年7月,貝達藥業以200萬美元收購MRX-2843在中國的權益,負責MRX-2843在中國的R&D和申報。
1類生物藥臨床審批概況
2019年1月,中國共有9個1類生物藥獲得NMPA臨床默示許可,其中2個為特批品種。具體信息如下表所示:
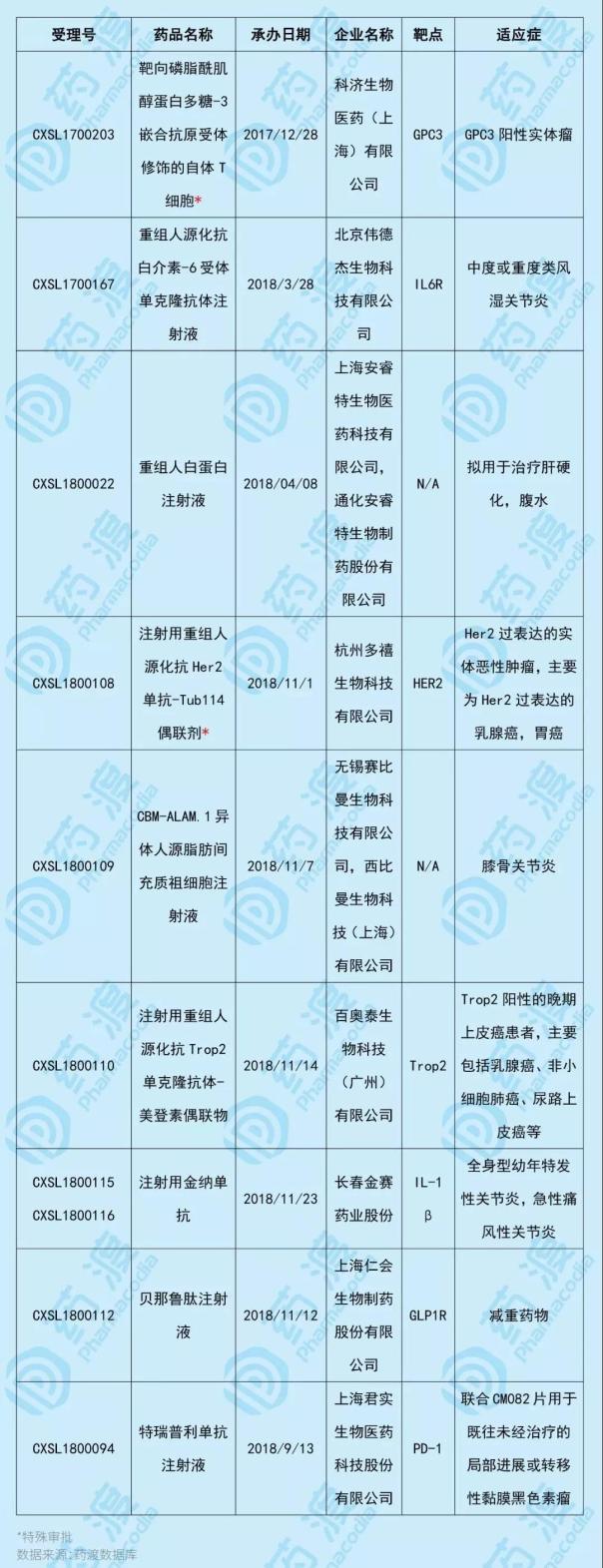
1、靶向磷脂酰肌醇蛋白多糖-3嵌合抗原受體修飾的自體T細胞GPC3-CAR-T cell)
GPC3-CAR-T細胞是一種嵌合抗原受體(CAR)T細胞療法,旨在治療肝細胞癌(HCC)、肺癌、乳腺癌和胃癌。磷脂酰肌醇蛋白聚糖-3(GPC3)是硫酸乙酰肝素蛋白聚糖(HSPG)家族的成員,其羧基末端通過糖基磷脂酰肌醇(GPI)錨定在細胞膜上。GPC3在肝癌細胞表面高表達,對癌細胞的粘附、增殖、侵襲和轉移具有重要意義。GPC3-CAR-T細胞可以介導GPC3陽性癌細胞的靶向殺傷作用。
該產品由科濟生物醫藥研發,與上海交通大學醫學院附屬仁濟醫院合作在國內進行一期臨床試驗。
2、重組人源化抗白介素-6受體單克隆抗體注射液
北京偉德杰生物科技研發的重組人源化抗IL -6受體單克隆抗體,擬用于治療中重度類風濕性關節炎。該藥物的IND申請由NMPA于2018年3月承擔,并于2019年1月獲得臨床暗示許可。
3、重組人白蛋白注射液
安瑞特生物技術公司開發的重組人白蛋白旨在用于治療肝硬化、腹水和其他適應癥。白蛋白主要由肝臟合成,具有維持血液滲透壓和營養載體的作用。傳統的血液制劑存在產量低、價格高、交叉污染等缺點。基因重組技術具有巨大的應用潛力。目前,我國同類型的中國一類新藥如下表所示:
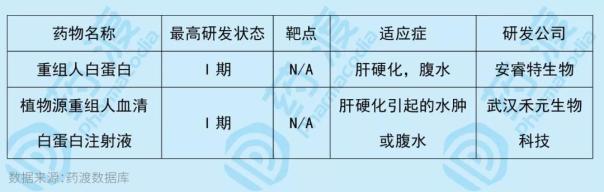
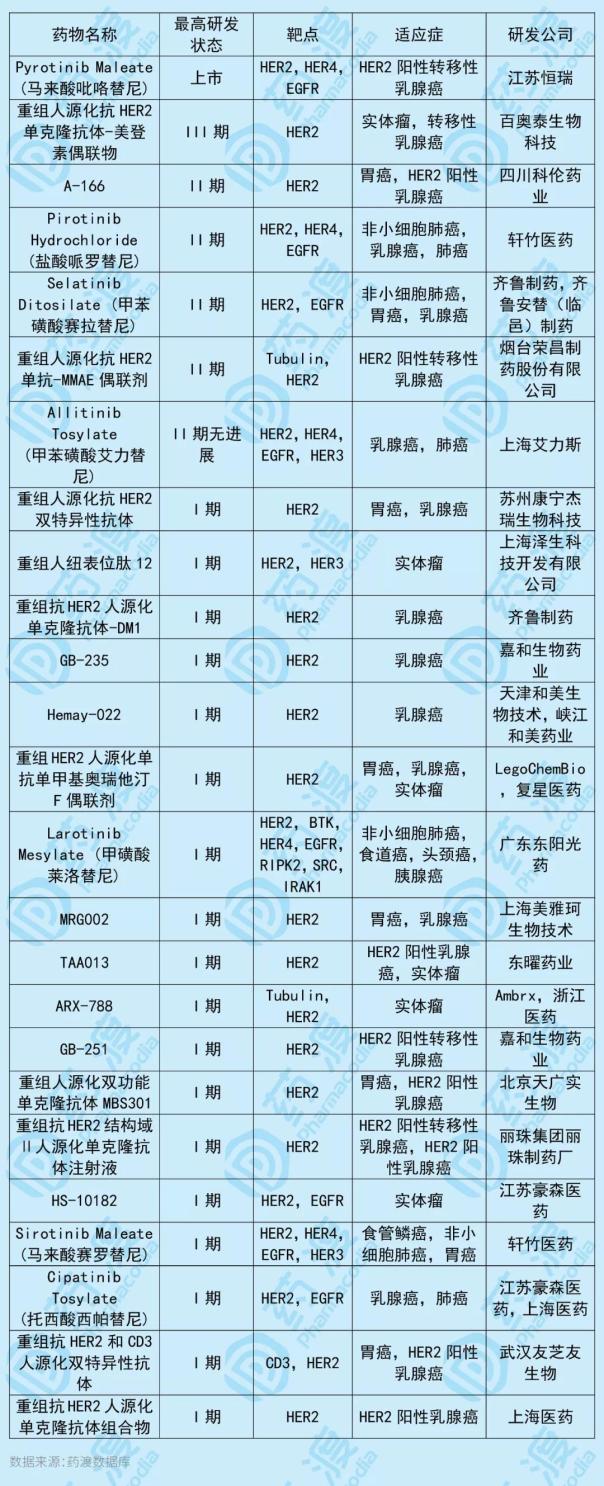
4、重組人源化抗Her2單抗-Tub114偶聯劑
-Tub114偶聯劑是杭州多喜生物醫藥研發的重組人源Her2單克隆抗體,是新一代高效低毒的抗體偶聯藥物(ADC)。它由重組人源化抗Her2抗體通過功能性接頭與微管溶素衍生物偶聯而成,將用于治療Her2陽性實體瘤,如Her2陽性乳腺癌、胃癌、結直腸癌、尿路上皮癌等。目前,具有相同目標的中國第一類新藥如下表所示:
5、異體人源脂肪間充質祖細胞注射液
Biman公司開發了一種基于同種異體人脂肪間充質祖細胞(AlloJoin)的干細胞治療藥物,擬用于治療膝關節骨關節炎。AlloJoin是中國第一個臨床批準的干細胞產品,將直接從二期臨床試驗開始測試。
6、注射用重組人源化抗Trop2單克隆抗體-美登素偶聯物
BAT-8003是BIOTAI公司開發的一種抗體偶聯的靶向腫瘤相關鈣信號傳感器2(Trop2)的藥物。它旨在用于治療Trop2陽性乳腺癌和胃癌。Trop2是一種滋養層細胞表面抗原,這種跨膜糖蛋白參與細胞內鈣信號轉導,與腫瘤細胞的增殖和侵襲有關。
7、金納單抗
Gennadizumab是一種抗白細胞介素-1-的人單克隆抗體,旨在用于治療系統性幼年特發性關節炎和急性痛風性關節炎。它是由長春金賽制藥有限公司研制的.
8、貝那魯肽注射液
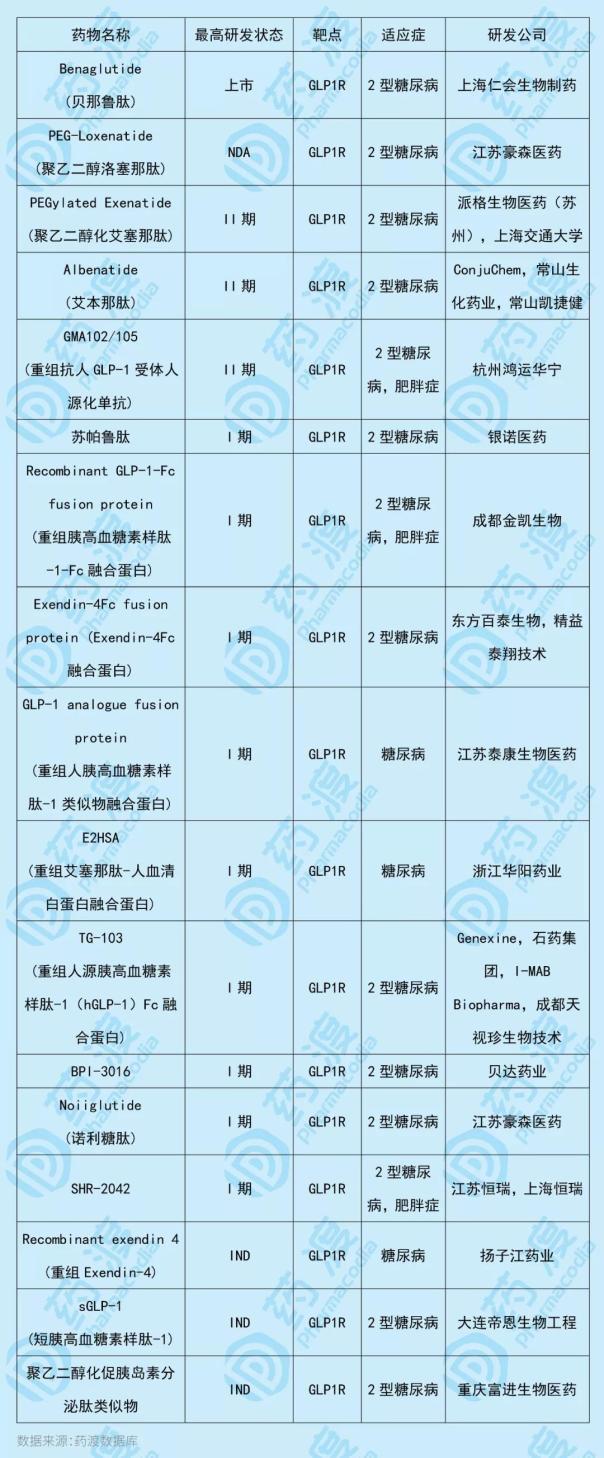
Bellutide是一種重組人胰高血糖素多肽-1(7-36),本質上是一種腸促胰島素分泌肽。作為GLP1受體的激動劑,促進葡萄糖依賴性胰島素的釋放并減少胰高血糖素的分泌。貝露肽由上海任慧生物制藥有限公司研發,于2016年12月13日獲得CFDA(現NMPA)批準。它被用來治療二型糖尿病,它的商品名稱是益生泰。在以糖尿病為適應癥的臨床研究中,苯那肽顯示出明確而顯著的減肥效果。此外,用于減肥適應癥的IND已于2016年7月獲得FDA批準。與那魯肽靶點相同的中國一類新藥如下表所示:
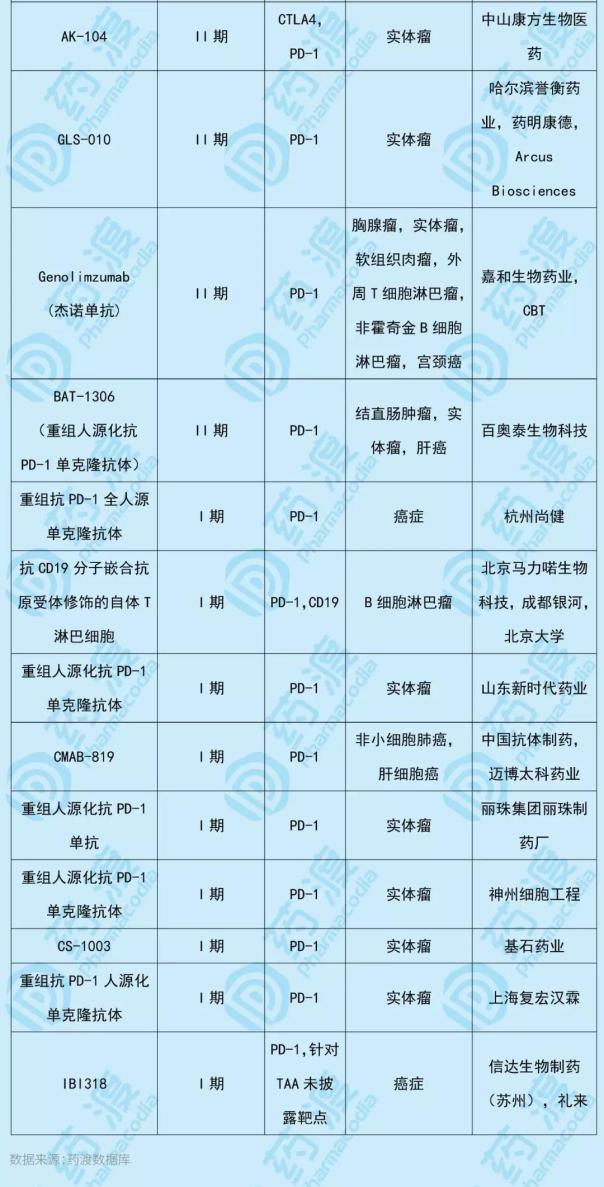
9、特瑞普利單抗注射液
Riplizumab (JS001)是一種人源化單克隆抗體,其靶向程序性死亡受體1(PD-1)。它旨在用于治療乳腺癌、淋巴瘤、惡性黑色素瘤、泌尿生殖器癌、肝細胞癌、食道癌和其他種類的實體瘤。2018年12月17日,NMPA有條件批準了曲普利單抗注射液的上市申請,用于治療既往全身治療失敗后不可切除或轉移性黑色素瘤患者。商品名為易拓,它成為第一個在中國獨立開發和銷售的PD-1單克隆抗體。此次申報適應癥為黏膜黑色素瘤,在中國具有相同靶點的1類新藥如下表所示:

中國1類新藥NDA申請概況
2019年1月,NMPA藥品檢測中心承擔了兩項1類n的NDA申請
澤麥布是一種膽固醇吸收抑制劑,通過作用于小腸刷狀緣轉運蛋白NPC1LI,抑制食物和腸道、肝臟中循環膽固醇的吸收。該藥由浙江海正公司研發,用于治療原發性高膽固醇血癥。
1、海澤麥布
2019年1月,NMPA承接了NDA的申請。
2018年9月,完成了2015年開始的兩項臨床III期試驗,以評估高膽固醇血癥患者單獨或聯合使用黑澤米的療效和安全性(NCT03413462,CTR20150787;NCT03464682,CTR20150351).
2014年,在美國和中國分別開展了期臨床研究NCT02087917和CTR20140489。
2012年11月,美國的IND申請獲得FDA批準。
2012年4月提交中國化學藥物1.1類IND申報,當年10月獲得臨床批準文件。
研發里程碑
2018年9月公布了支持高膽固醇血癥患者單一藥物上市的Heizemib的兩項關鍵臨床III期試驗(CTR20150787,CTR20150351)的結果。這兩項試驗分別是多中心、隨機、雙盲、安慰劑對照的期臨床試驗和開放的長期安全性觀察研究(以下簡稱“單藥期試驗”),觀察黑色麥布(HS-25)治療原發性高膽固醇血癥的療效和安全性,以及黑色麥布(HS-25)聯合阿托伐他汀治療動脈粥樣硬化性心血管疾病等危重疾病的隨機、雙盲、雙模擬、多中心觀察。兩項試驗的主要療效指標為12周時低密度脂蛋白(LDL-C)的下降率。結果表明,兩項試驗均達到預設標準,療效與文獻報道的依澤替米貝相當,不良反應輕微,安全性良好。
總共有374名受試者參加了單個III期試驗。與安慰劑組相比,LDL-C的主要療效指標下降了-14.6%(FAS組)和-16.0%(PPS組)。不良反應與安慰劑無統計學差異,短期和長期用藥安全性良好。共有255名受試者參加了中間III期試驗。對于常規他汀類藥物治療未達到目標值的動脈粥樣硬化性心血管疾病和其他危險疾病的高膽固醇血癥患者,在10mg阿托伐他汀作為背景治療的基礎上,增加一倍的黑澤米或阿托伐他汀劑量,通過FAS set分析LDL-C黑澤米降低-16.4%(PPS set為-16.8%,sub-2。在安全性方面,黑澤麥布和阿托伐他汀的不良反應發生率分別為7.9%和13.6%,黑澤麥布和阿托伐他汀的總體不良事件和不良反應頻率均低于阿托伐他汀。一個
參考數據
1.海正藥業股份有限公司:關于公司產品海澤麥布(Pro。2018-106)
臨床結果
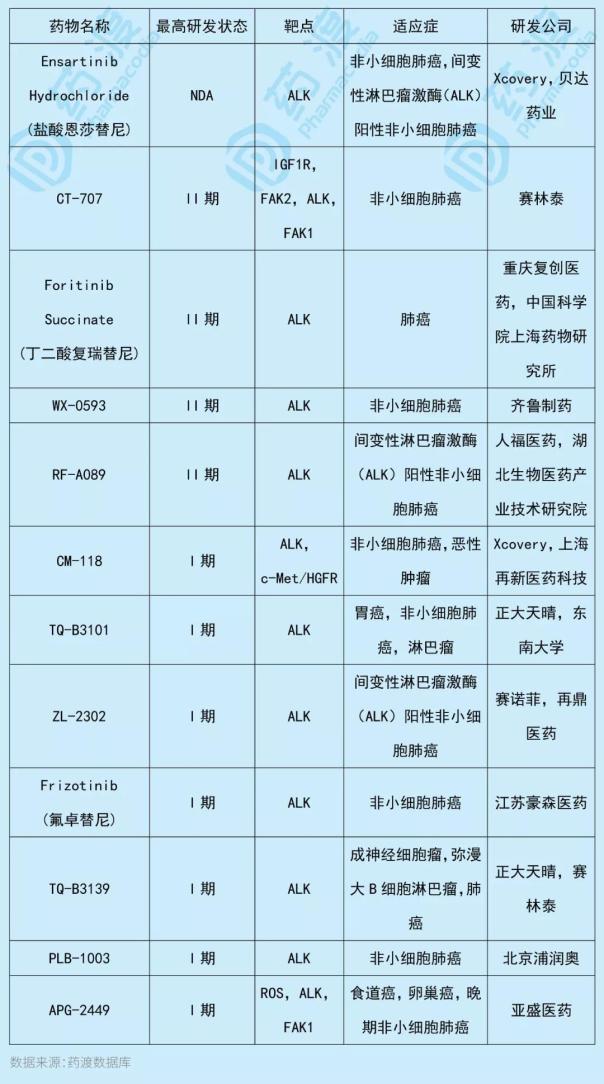
鹽酸恩替尼是一種小分子變性淋巴制造酶ALK抑制劑,它也對TRKA融合、TRKC、ROS1、EphA2和c-MET具有潛在的抑制活性。ALK與染色體重排有關,其異常表達是一些非小細胞肺癌的主要標志和有效靶點。該藥最初由Xcovery研發,2014年授權給貝達藥業用于治療NSCLC。
2、鹽酸恩莎替尼
2018年12月26日,NMPA承接了NDA申請。
2016年6月,在美國、歐洲、澳大利亞、中國香港、以色列、韓國和土耳其開始了在ALK陽性非小細胞肺癌患者(n=402)中比較恩替尼和克唑替尼的III期研究(NCT02767804、X396-CLI-301、eXalt3、CTR20170919 ),該研究于2017年4月在日本開始,而在2018年8月,該研究仍在美國、歐洲、韓國進行
2016年10月,貝達藥業、Xcovery、Cotalent在中國提交的臨床申請(進口一類)由NMPA承擔,2017年5月獲準開展全球多中心臨床期試驗。
2015年11月,貝達藥業向NMPA提交了中國化學藥1.1類臨床研究,并于2016年8月獲得臨床試驗批文。
2012年6月,在美國啟動了針對晚期實體瘤和非小細胞肺癌患者(n=100)的開放標簽、劑量遞增的臨床I期研究(NCT01625234,X396-CLI-101,eXalt2)。
研發里程碑
2017年5月,在ELCC會議上公布了關于晚期實體瘤和非小細胞肺癌患者治療的臨床II期研究的eXalt2數據。結果顯示,10例患者(9例為靶病變,1例僅為非靶病變)顱內反應的中位持續時間大于5.8個月,最長持續時間為24個月。一個
2018年3月,發表了ensatinib的I/II期臨床數據。結果表明,對于新診斷的ALK陽性肺癌患者,恩替尼的有效率高達80%;對于克唑替尼耐藥的患者,有效率高達69%。2
2018年6月,治療中國ALK陽性非小細胞肺癌的I期臨床結果:22例患者入選,8例患者出現3級或以上不良反應,主要為皮疹(27.3%)。在14例可評價療效的患者中,9例為PR,3例為SD。三
2018年6月,eXalt3研究成果在ASCO會議上公布。這項研究在20個國家和98個測試中心進行。在這項全球多中心、開放標簽、隨機分配的研究中,約有270名非小細胞肺癌患者,他們以前沒有接受過ALK TKI(ALK酪氨酸激酶抑制劑),以前最多接受過一個化療方案,并且ALK陽性。患者隨機接受恩替尼(225 mg,每天一次)或克唑替尼(250 mg,每天兩次),直到疾病進展或毒性無法耐受。研究表明,恩替尼在PFS療效指數上優于克唑替尼的概率為80%(雙側水平為0.05)。四
參考數據
1.ELCC 2017新聞:Ensartinib在ELCC 2017/05 ALK陽性非小細胞肺癌患者中證明了CNS活性。
2.Horn L,Infante J R,Reckamp K L,et (X-396)在ALK陽性非小細胞肺癌中的應用:一項首次在人類進行的I/II期多中心研究結果[J].2018年臨床癌癥研究:
3.Ensartinib (X-396),第二代ALK TKI,中國ALK陽性非小細胞肺癌:一項I期,劑量遞增研究,ASCO,2018/06。
4.exalt 3:ACSO,2018/06,在間變性淋巴瘤激酶(ALK)陽性非小細胞肺癌(NSCLC)患者中比較沙替尼和克唑替尼的3期隨機研究。
與恩替尼作用靶點相同的中國一類新藥如下表所示: