PIC/S是1995年11月建立的藥品檢查合作計劃的縮寫。是世界上唯一由GMP檢查和執法機構組成的國際合作組織。PIC/S的目的是消除藥品貿易中的障礙,提高藥品獲得行政許可的一致性,保證藥品質量,促進國際GMP法規標準的協調和GMP檢驗質量的一致性。
PIC/S成立于1970年(藥品檢驗公約,簡稱PIC);PIC的章程與PIC/S不同,PIC是國家作為成員單位簽署成立的正式國際組織,一直運作到1995年歐盟成立。最終,PIC受到歐盟體系的限制,無法與其他希望加入的國家簽署協議,于是催生了另一個非正式的、更加靈活的國際合作組織PICS,如今PIC與PICS(統稱PIC/S)并行運作,致力于推動GMP的國際合作和檢驗標準的統一。
2018年1月1日,新加坡衛生科學局(HSA)的Boon Meow Hoe先生成為PIC/S的第23任主席(圖1),這是PIC/S歷史上第一次由亞洲人擔任主席。他的任期為兩年(2018-2019)。PIC/S在全球享有很高的聲譽,近年來影響力不斷擴大;此外,隨著歐美互認協議的生效,全球GMP標準的一致性趨勢越來越明顯。PIC/S成員有一致的GMP標準和檢驗體系,并根據雙方協議決定是否承認對方的檢驗結果。盡管PIC/S成員并不完全認可GMP認證結果,但中國制藥企業積極學習PIC/S法規和指南對于更好地了解國際監管環境和國際貿易規則是非常有益的。
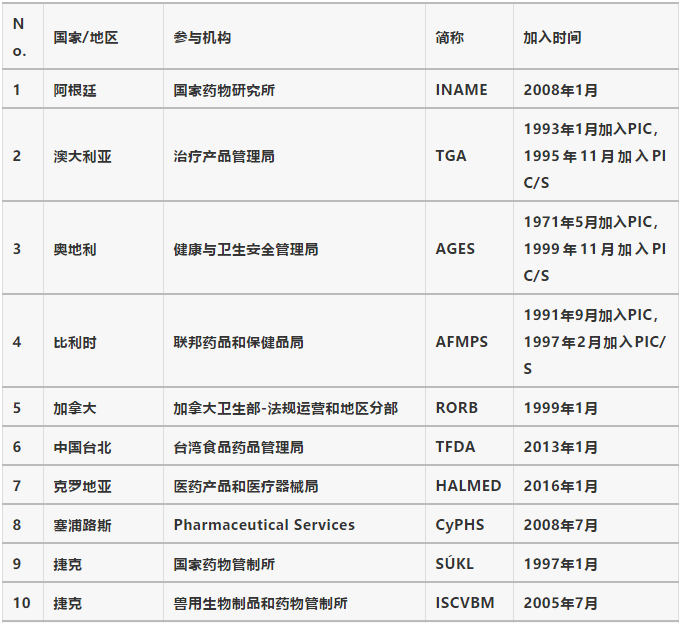
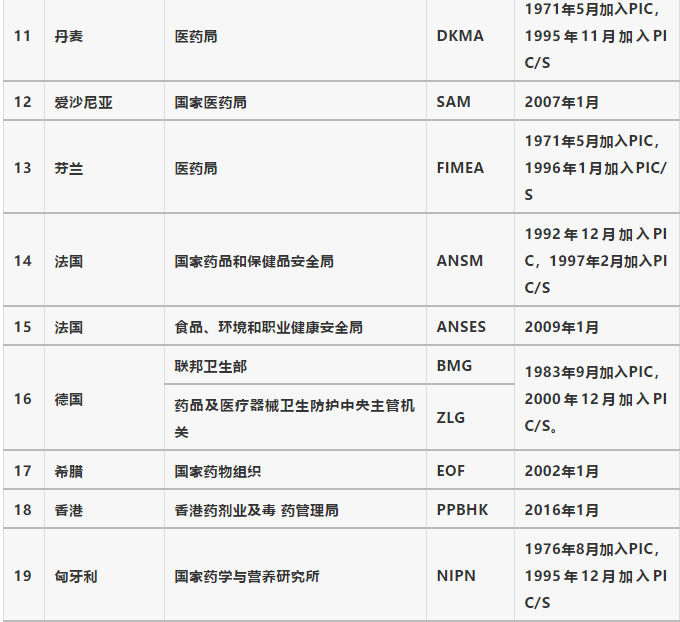
加入PIC/S成員的一個基本要求是其藥品監管機構能夠采用與PIC/S相同的GMP檢查體系,其要求和程序能夠保證GMP檢查體系的實施和相互合作。應根據PIC/S聯合評估項目或等效項目對各成員的檢驗系統進行重新評估。目前,PIC/S擁有來自49個國家或地區的52個成員,包括阿根廷、澳大利亞、奧地利、比利時、加拿大、中國臺北、克羅地亞、塞浦路斯、捷克、丹麥、愛沙尼亞、芬蘭、法國、德國、希臘、中國香港特別行政區、匈牙利、冰島、印度尼西亞、伊朗、愛爾蘭、以色列、意大利、日本、韓國、拉脫維亞、列支敦士登、立陶宛、馬來西亞、馬耳他、墨西哥、日本。羅馬尼亞、新加坡、斯洛伐克、斯洛文尼亞、南非、西班牙、瑞典、瑞士、泰國、土耳其、烏克蘭、英國和美國的主要藥品管理局,其中捷克共和國的sKL和ISCVBM、法國的ANSM和ANSES以及英國的MHRA和VMD分別作為兩個獨立機構加入。(詳見圖2和表1)。
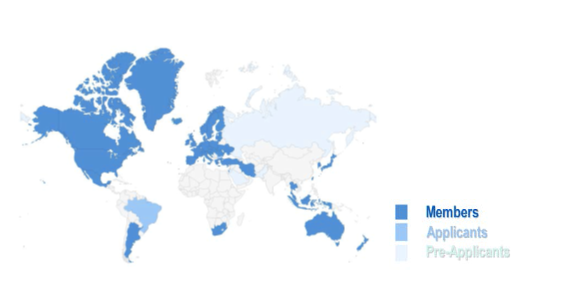
圖2 PIC/S成員機構分布
表1 PIC/S成員機構清單
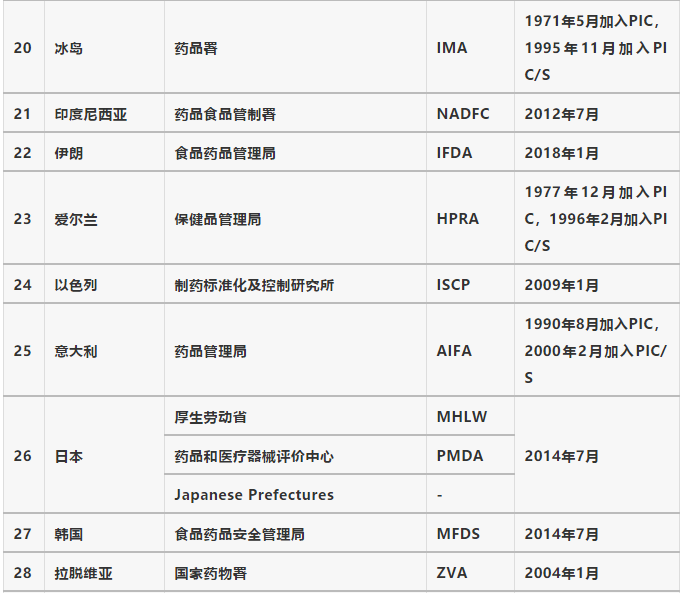
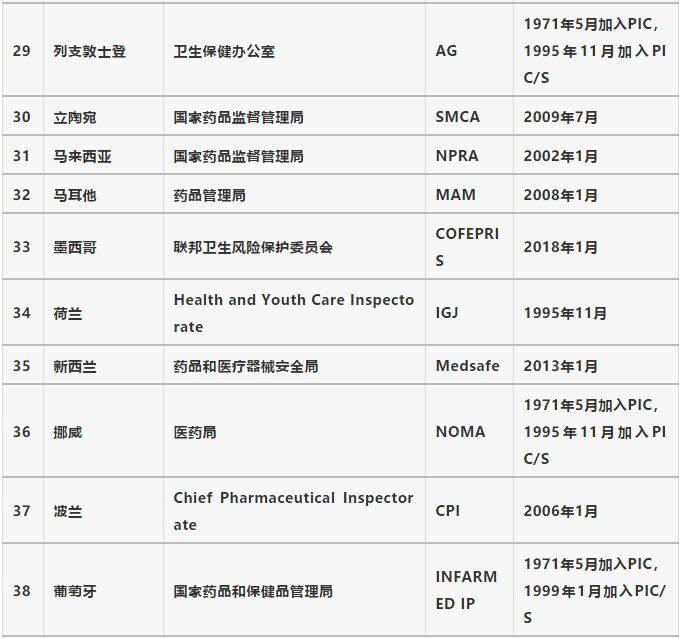
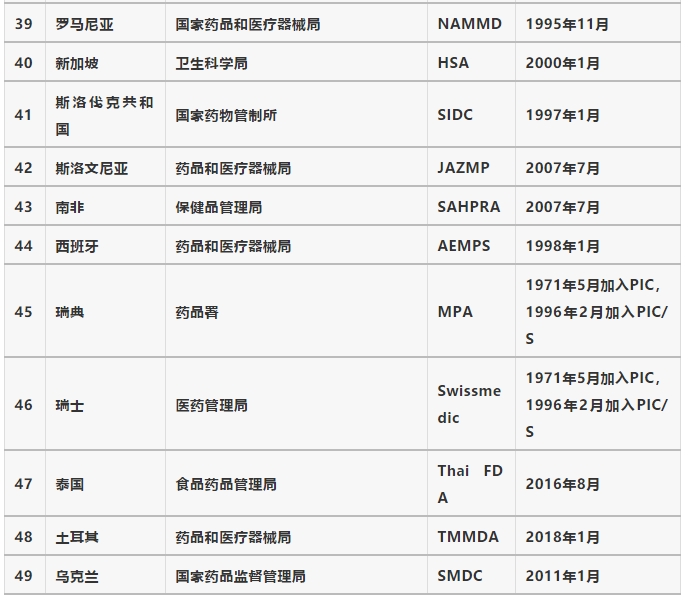

PIC/S有三個職能機構:委員會、執行委員會和秘書處。自2014年以來,PIC/S在以下領域設立了七個小組委員會:培訓(SCT)、專家組(SCEC)、戰略發展(SCSD)、合規(SCC)、全球機制(D)P協調(SCH)、預算、風險和審計(SCB)以及溝通(SC COM)(詳見圖3)。
GMP檢查員培訓是PIC/S的一項重要活動。PIC/S的目的之一是促進國際GMP法規和標準的協調以及GMP檢查質量的一致性。通過PIC/S GMP指南協調GMP要求不足以保證GMP的統一解釋和應用,因此GMP檢查員的培訓是實現這一目標的必要工具。最近,PIC/S還為活躍在國內生產總值、GCP和GVP等其他領域的檢查員開設了培訓課程。2018年,PIC/S舉辦的系列培訓如下:
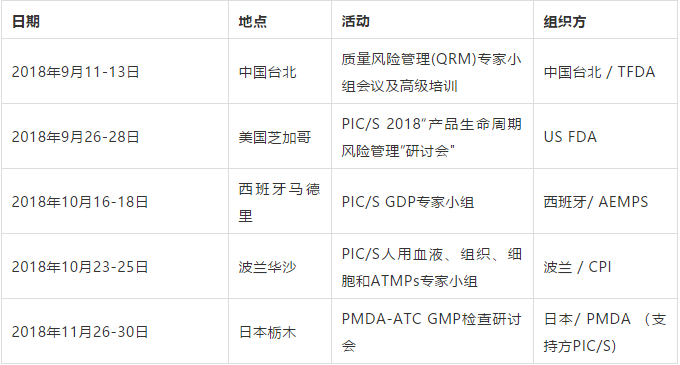
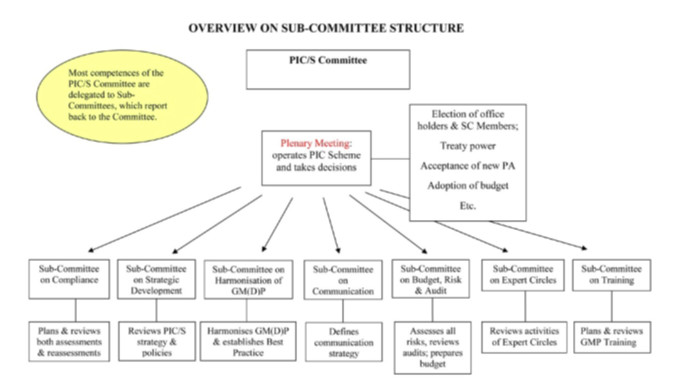
圖3 PIC/S組織結構圖
GMP與GDP的協調是PIC/S的核心,采用共同標準的主要原因是:保證藥品質量,促進藥品行政許可的一致性,促進檢驗的一致性和統一性,促進醫藥產品貿易壁壘的消除。這些就是PIC/S的宗旨,SCH包括七個工作組,分別是GMP附件1無菌生產工作組、GMP附件2修訂工作組、數據完整性工作組、GMP缺陷分類協調工作組、共用設施交叉污染控制工作組、PIC/S血液指南文件修訂工作組、PI 006驗證修訂工作組。
SCH的主要職責之一是協調歐盟的GM(D)P指導文件,特別是PIC/S GMP指南和附件,并將歐盟的修訂文件轉化為PIC/S自己使用。2018年SCH協調轉換的文件包括:對PIC/S GMP指南第三章(設施設備)、第五章(生產)、第八章(投訴和產品召回)進行了修訂,并于2018年7月1日生效;將歐盟GMP附錄13(臨床試驗用藥物)修訂版改為PIC/S版,2019年提交征求意見;本文討論了將歐盟附件16(QP人員認證和批簽發)修改為PIC/S版本的建議。此外,PIC/S專家還參與了EMA起草組對EU-PIC/S GMP指南以下章節和附件的修訂:第1章(藥品質量體系)、第4章(文件)和附件11(計算機化系統)、附件1(無菌制造)、附件17(實時放行試驗、原始參數放行)和附件21(輸歐盟進口藥品的GMP責任)。
PIC/S專家組由PIC/S委員會設立,旨在促進特定GMP領域(如血液、計算機化系統、原料藥、質量風險管理、共用設施交叉污染、GDP、GCP、GVP等)檢查員之間的討論和信息交流。).專家組會議定期起草指導意見和建議,并在各自的專業領域提供培訓。
2017年6月,中國CFDA加入ICH后,中國藥品監管邁出了R&D國際化和注冊化的歷史性一步,藥品走出國門的步伐將進一步加快。然而,在藥品生產監管領域,中國的監管體系尚未實現與歐美其他主流國家的互認。PIC/S前主席Paul Hargreaves在2016年舉行的PDA/FDA聯合年會上提到,“中國多年來一直表達了加入PIC/S的興趣,PIC/S也與CFDA進行了會面……”。此外,PIC/S PIC/S 2019的工作計劃中明確表示將與非成員主管機關建立(或保持)密切聯系,這些機構表示有興趣加入PIC/S,尤其是中國/NMPA和印度;此外,PIC/S將繼續加強與中國/NMPA的合作。
下表列出了與中國藥品監管和PIC/S組織相關的主要事件:

通過對以上信息的總結和分析,作者得出結論:中國美國食品藥品監督管理局(NMPA)加入PIC/S還需要很長時間,原因一是中國大陸各省之間監管水平差距較大。除傳統醫藥大省、長三角大省和珠三角大省監管能力較強外,其他省份實施PIC/S GMP監管制度存在現實困難。第二個原因是政治考慮。畢竟,中國臺灣省和中國香港都是PIC/S的成員,如何處理它們之間的關系需要中國美國食品藥品監督管理局(NMPA)慎重考慮。
參考資料:
1-PIC/S 2018年度報告
2- PIC/S官方網站信息
原標題:展望| PIC/S組織影響力持續擴大,中國NMPA入世進程最新展望