9月20驲正在CSCO年會上,上海復(fù)星醫(yī)藥控股子公司復(fù)宏漢霖自立研發(fā)的生物近似藥利妥昔單抗(HLX-01)頒布要害3期臨床數(shù)據(jù),HLX-01與原研藥(美羅華)正在醫(yī)治CD20陽性彌漫型年夜B非霍奇金淋巴瘤初治患者的臨床試驗次要盡頭、主要盡頭(安全性、免疫原性、藥代動力學(xué))均到達(dá)預(yù)設(shè)尺度。HLX-01是現(xiàn)階段獨一一個處于上市審評階段的利妥昔單抗生物近似藥。
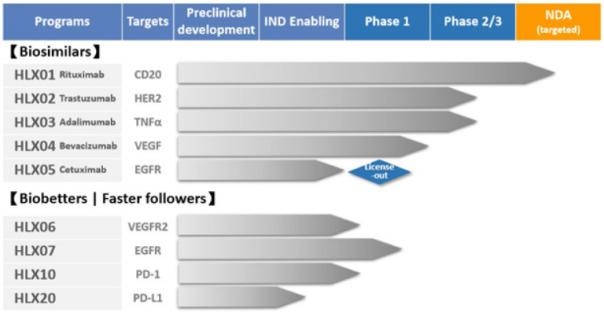
筆者匯總了HLX-01跟原研藥正在DLBCL適應(yīng)癥的臨床數(shù)據(jù),并借助此文剖析了現(xiàn)階段海內(nèi)CD20單抗的開辟跟注冊申報希望。
1、首款海內(nèi)自立研發(fā)利妥昔單抗HLX-01行將上市
2017年10月30驲,CFDA受理復(fù)宏漢霖HLX-01上市請求(CXSS1700026)該審評歸入第26批優(yōu)先審評目次,現(xiàn)階段該產(chǎn)物已實現(xiàn)技巧審評跟三合一審評。除彌漫性年夜B細(xì)胞淋巴瘤適應(yīng)癥中,類風(fēng)濕關(guān)節(jié)炎處于3期臨床。
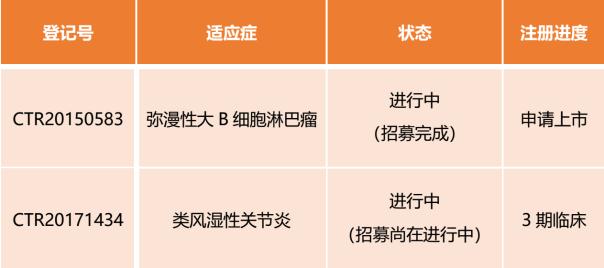
2018年09月20驲,CSCO年會上,上海復(fù)星醫(yī)藥控股子公司復(fù)宏漢霖自立研發(fā)的HLX-01頒布要害3期臨床數(shù)據(jù)。
要害3期臨床數(shù)據(jù):HLX-01的3期臨床研討是一項隨機、雙盲、平行對比的多中間(33家)臨床試驗(CTR20150583,NCT02787239),該研討招募患者407例,評估生物近似藥與原研藥作為彌漫型年夜B非霍奇金淋巴瘤一線療法的安全性跟有效性。
利妥昔單抗注射液與原研藥(美羅華)正在醫(yī)治CD20陽性彌漫型年夜B非霍奇金淋巴瘤初治患者的臨床試驗次要盡頭、主要盡頭(安全性、免疫原性、藥代動力學(xué))均到達(dá)預(yù)設(shè)尺度。
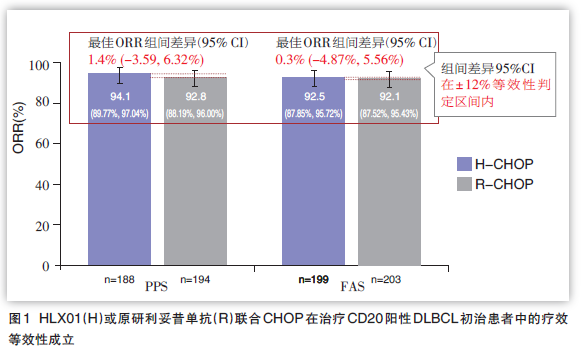
揭盲后療效成果圖表
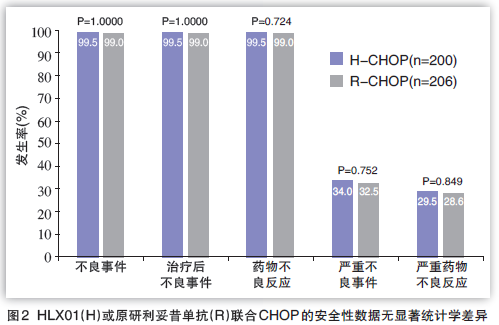
揭盲后安全性成果圖表
2、海內(nèi)CD20單抗藥物匯總剖析
筆者依據(jù)公然渠道,收拾整頓了現(xiàn)階段海內(nèi)正在注冊申報的CD20單抗藥物,此中,海內(nèi)已上市2款,原研產(chǎn)物羅氏美羅華(利妥昔單抗)海內(nèi)已上市18年;三生國健利妥昔單抗生物近似藥曾報產(chǎn)(撤回),5款處于3期臨床,9款處于1期臨床。
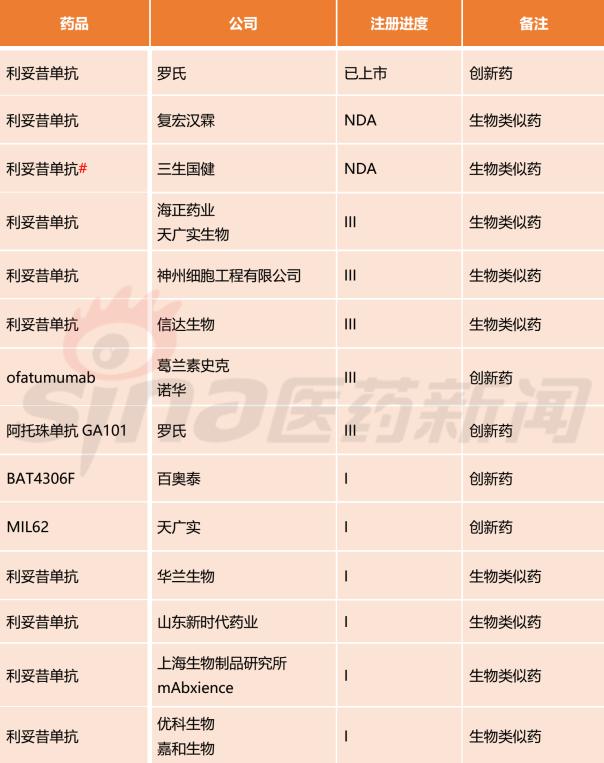
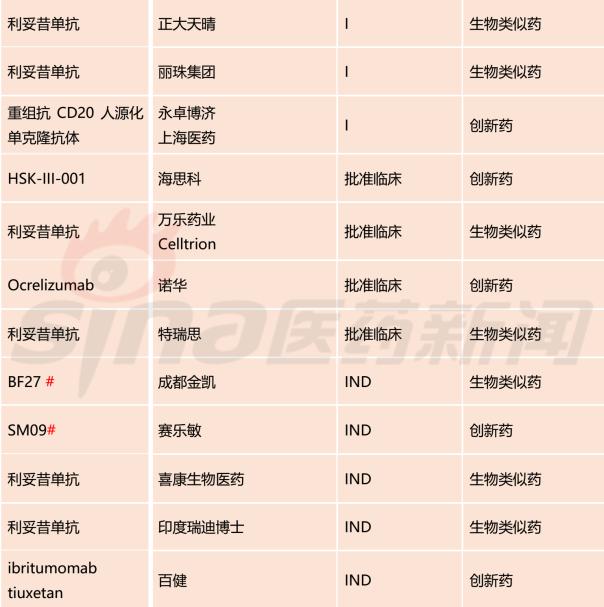
備注:#為自動撤回
海內(nèi)正在申報的CD20單抗25款種類中,生物近似藥16款,翻新藥9款,筆者正在這里不再比照各翻新藥的序列差別,行業(yè)內(nèi)讀者可以對相關(guān)抗體做更加深化的剖析,如9款抗體藥物的要害數(shù)據(jù),包羅安全性、免疫原性跟臨床有效性數(shù)據(jù)。
遠(yuǎn)段時間,國產(chǎn)抗體生物近似藥連續(xù)報,雖然中國生物近似藥上市的工夫晚于歐盟跟美國多年,可是,首款美羅華的上市將依舊意思不凡。
2017年醫(yī)保準(zhǔn)入會談后,利妥昔單抗500mg/50ml的價錢為8290元人民幣,貶價幅度高達(dá)58.45%,年用度正在18.6萬人民幣。
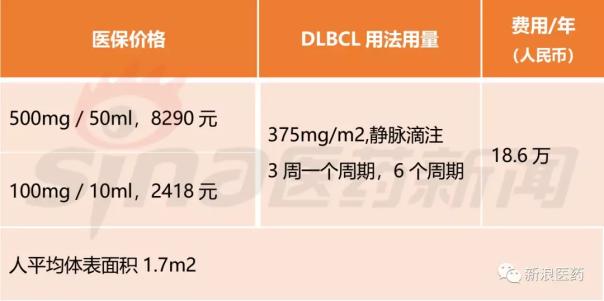
那么,國產(chǎn)美羅華將會若何訂價?迎接留言交換。