系統性紅斑狼瘡簡介
系統性紅斑狼瘡(SLE)是自身免疫介導的,以免疫性炎癥為突出表現的彌漫性結締組織病,好發于生育年齡女性。血清中出現以抗核抗體為代表的多種自身抗體和多系統受累是SLE的兩個主要臨床特征。
在美國多地區的流行病學調查報告顯示,SLE的患病率為14.6~122/10萬人;我國大樣本的一次性調查(3萬人)顯示SLE的患病率為70/10萬人,婦女中則高達113/10萬人。SLE為兒童常見風濕性疾病之一,兒童的發病率國外報道為(0.36~0.60)/10萬人,亞洲地區的日本報道每年患病率為0.47/10萬人,我國臺灣地區16歲以下兒童患病率為6.3(5.7~7.0)/10萬人。目前尚無我國大陸地區兒童SLE發病率或患病率的報道,但小樣本的病例顯示男女患病比例為1:(3.9~5.93)。
SLE病情輕重程度分類:1)輕型SLE:指SLE診斷明確或高度懷疑者,但臨場穩定且無明顯內臟損害。2)中型SLE:指有明顯重要臟器受累及且需要治療的患者。3)重型SLE:指狼瘡累及重要臟器。4)狼瘡危象:指危及生命的重癥SLE,如急進性LN、嚴重的中樞神經系統損害、嚴重的溶血性貧血等。
治療藥物
對于該病目前還沒有根治的辦法,僅能達到病情緩解,治療原則為積極控制狼瘡活動、改善和阻止臟器損害。常用藥物主要有糖皮質激素、免疫抑制劑、抗瘧藥和非甾體抗炎藥等。除此之外還可使用生物制劑,如利妥昔單抗、貝利木單抗。
1)利妥昔單抗
利妥昔單抗(Rituxan、Rituximab)由百健和羅氏聯合研發,于1997年11月26日獲得FDA批準,1998年6月2日獲得EMA批準,2008年獲得CFDA批準上市。利妥昔單抗是人鼠嵌合的抗B淋巴細胞CD20的單克隆抗體, 在體內能有效清除異常增生的B淋巴細胞。該藥批準的適應癥為非霍奇金淋巴瘤、慢性淋巴細胞白血病、類風濕性關節炎、肉芽腫血管炎和顯微鏡下多血管炎。雖然利妥昔單抗未被批準用于治療系統性紅斑狼瘡,但B細胞功能障礙被認為是SLE發病機制中最重要的一環, CD20是B細胞特異的表面標記物。2012年美國風濕病協會(ACR)指南建議,在誘導治療6個月后腎炎未得到改善甚至惡化的LN 患者,或CTX和MMF治療均失敗的患者,可考慮使用利妥昔單抗。
2)貝利木單抗
貝利木單抗(Benlysta、Belimumab)由葛蘭素史克研發,于2011年3月9日獲得FDA批準,是50年來所批準的第一個治療系統性紅斑狼瘡的新藥,隨后在2011年7月13日該藥也獲得了EMA批準上市。該藥目前還未在中國上市,正在開展3期臨床試驗。
貝利木單抗是一種單克隆抗體藥物,可以結合并抑制一種稱為B-淋巴細胞刺激因子(BLyS)的蛋白,阻斷BLyS可引起B細胞自我破壞,使人體的免疫系統停止攻擊自身組織。Belimumab能夠減少導致狼瘡患者病情加重的異常B淋巴細胞的數量,這些異常的B淋巴細胞會導致免疫系統產生細胞錯誤攻擊血管和自身其他健康組織,從而引起狼瘡和其他免疫系統疾病。GSK于2016年9月宣布已向美國FDA提交皮下注射劑Belimumab的生物制品許可申請(BLA)和向EMA提交了擴大的上市許可申請(MAA)。
新藥研發情況
SLE治療領域的藥物開發極具有挑戰性,失敗率很高,而目前進入三期的藥物也較少。下面對全球進入臨床三期及國內企業研發的藥物進行簡單介紹:
1、Anifrolumab(MEDI546,MDX-1333, MEDI-546)
Anifrolumab由Medlmmune(阿斯利康的子公司)研發,是一種靶向1型干擾素受體的單克隆抗體,目前在國外處于臨床三期研究階段,用于治療中度至重度、自身抗體陽性的系統性紅斑狼瘡。根據Anifrolumab完成的2期試驗結果,300 mg 劑量的 Anifrolumab 經 169 天治療后在 34.4% 的人中產生響應,而治療一年后,這種治療響應上升到逾50%。2017年11月,CFDA批準其開展臨床試驗。
2、Arteether Amine Maleate (馬來酸蒿乙醚胺、SM934)
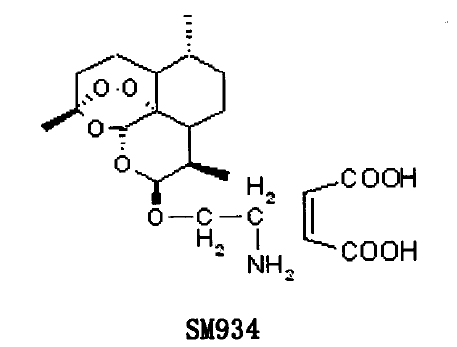
馬來酸蒿乙醚胺由中科院上海藥物研究所研發,用于治療系統性紅斑狼瘡,該藥品于2015年獲得中國化藥1.1類臨床批件,目前正在開展臨床一期試驗。
SM934在成藥性方面具有傳統青蒿素衍生物不具備的特點和優勢:水溶性高、口服吸收好,作為口服制劑給藥方便、毒性低。根據文獻對SM934治療系統性紅斑狼瘡作用機制的報道。SM934在體內和體外實驗中對T細胞介導免疫反應均表現出顯著抑制活性。SM934的免疫抑制活性可能與其抑制T細胞、誘導活化的T細胞凋亡、促進調節性T細胞分化有關。
3、雙氫青蒿素
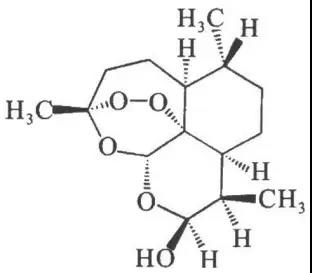
雙氫青蒿素(DQHS)新增SLE適應癥的臨床申請由中國中醫科學院中藥研究所于2016年1月正式提出,2016年3月已經獲得了藥監局臨床批準,目前由昆藥集團開展臨床二期試驗。根據文獻對DQHS治療SLE作用機制的報道,其能明顯改善BXSB小鼠LN的病理狀態。另外,DQHS通過抑制B淋巴細胞增殖,促進CD4T細胞和CD8T細胞的增殖,尤其是CD8T細胞增殖明顯,減少B細胞分泌自身抗體,從而達到治療紅斑狼瘡的作用。
4、重組人源化抗BLyS單克隆抗體注射液(UBP-1213)
UBP-1213是一種人源化單克隆抗體,靶向于B淋巴細胞刺激因子(BLyS)抑制劑,用于治療系統性紅斑狼瘡。該藥最初由武漢華鑫康源生物醫藥開發,之后上海眾合醫藥(被上海君實生物醫藥并購)獲得了該藥,目前由上海君實生物醫藥進行研發。UBP-1213由蘇州眾合醫藥(上海眾合醫藥的子公司)于2005年10月向國家食品藥品監督管理總局提交臨床試驗申請(重組人源化抗BLyS單克隆抗體注射液,治療用生物制品1類新藥),并于2016年11月獲得化藥1.1類臨床批件。
5、AC0058TA
AC0058TA由艾森生物研發,用于治療系統性紅斑狼瘡和類風濕性關節炎的魯頓酪氨酸激酶(BTK)抑制劑。該化合物2016年2月向國家食品藥品監督管理總局提交臨床試驗申請(AC0058TA膠囊、AC0058TA,化藥1.1類),并于12月獲得臨床批件。同時,AC0058TA還獲得了美國FDA的批準,目前正在開展1期臨床試驗(2016年7月登記)。
6、HMPL-523
HMPL-523由和記黃埔醫藥研發,用于治療風濕性關節炎,系統性紅斑狼瘡和多發硬化癥的脾酪氨酸激酶抑制劑。該化合物2015年7月向國家食品藥品監督管理總局提交臨床試驗申請(HMPL-523乙酸鹽片、HMPL-523乙酸鹽,化藥1.1類),目前處于在臨床一期狀態。但查詢中國臨床試驗數據庫,其開展的臨床試驗題目為HMPL-523治療復發或難治的成熟B細胞腫瘤的I期研究,與系統性紅斑狼瘡無關。同時,HMPL-523臨床一期試驗于2014年6月在澳大利亞啟動,適應癥為自身免疫性疾病。
B細胞是免疫系統的重要組成部分,在多種免疫系統疾病起到至關重要的作用,如類風濕性關節炎、系統性紅斑狼瘡及過敏等自身免疫疾病,以及包括淋巴瘤和白血病在內的血液腫瘤(即B細胞惡性腫瘤)。HMPL-523是針對B細胞受體信號通路中重要的組成部分-酪氨酸激酶Syk的小分子口服制劑。在臨床前研究中,HMPL-523顯現出良好的藥效和激酶選擇性,在關節炎動物模型上,它能有效逆轉關節炎癥及骨侵蝕,減少多種促炎性細胞因子的生成,并在動物的毒理學研究中顯示出良好的安全性。
7、Terrymitt Sodium (泰瑞米特鈉)
泰瑞米特鈉由蘇州長征-欣凱制藥(江蘇吳中醫藥控股子公司)和欣凱醫藥共同研發,用于治療系統性紅斑狼瘡和風濕性關節炎的藥物。該化合物2013年1月向國家食品藥品監督管理總局提交臨床試驗申請( 泰瑞米特鈉片、泰瑞米特鈉,化藥1.1類),于2014年10月獲得化藥1.1類臨床批件。目前處于在臨床一期狀態。
8、RCT-18 (重組人B淋巴細胞刺激因子受體-抗體融合蛋白)
RCT-18是煙臺榮昌制藥股份有限公司開發的一種融合蛋白,由跨膜激活劑及鈣調親環素配體相互作用分子(TACI)的BLyS/APRIL結合區和人免疫球蛋白Fc片段融合而成。該藥目前處于臨床三期研究階段,用于治療類風濕性關節炎和系統性紅斑狼瘡。
總結
系統性紅斑狼瘡的治療繼2010版中華醫學會風濕協會《系統性紅斑狼瘡診斷及治療指南》后,在近6年的時間內無重大變化,SLE的治療仍以糖皮質激素、免疫抑制劑、抗瘧藥為主。其中2011年批準上市的貝利木單抗為50年來FDA所批準的第一個治療SLE的新藥。SLE的治療藥物中大部分常用藥物均屬于超說明書用藥,如免疫抑制劑、利妥昔單抗、卡托普利、長春新堿等。而查詢在研藥物情況,也發現SLE治療領域的藥物開發在全球藥企中都具有極高的挑戰性,研發失敗率很高(占總研發藥物的50%)。
參考:
1、系統性紅斑狼瘡診斷及治療指南(2010,中華醫學會風濕病協會)
2、兒童系統性紅斑狼瘡診療建議(2011,中華醫學會)
3、侯立飛.青蒿素衍生物SM934治療系統性紅斑狼瘡藥效及機制研究.中國科學院大學, 2009
4、藥渡數據庫