1月19日,國家美國食品藥品監(jiān)督管理局發(fā)布通報,經(jīng)中國食品藥品檢驗所檢驗,江蘇富源中藥飲片有限公司等8家企業(yè)生產(chǎn)的8批次中藥飲片被檢出不合格。其中,有一批藥品被廠家貼上標(biāo)簽,否認(rèn)是廠家生產(chǎn)的。
現(xiàn)將有關(guān)情況公布如下:
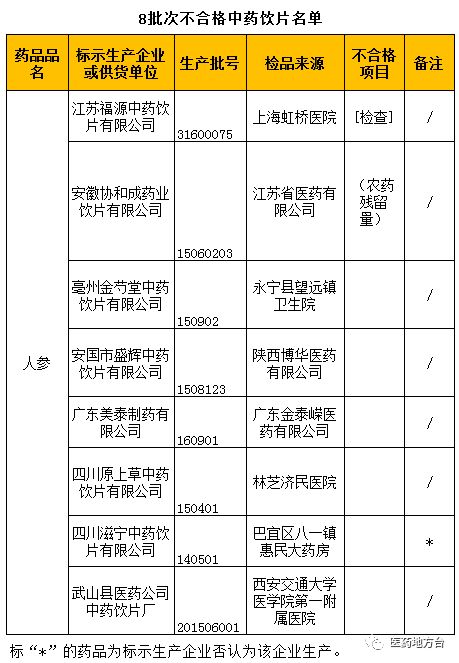
經(jīng)中國食品藥品檢驗所檢驗,標(biāo)稱江蘇富源中藥飲片有限公司、安徽協(xié)和成藥業(yè)飲片有限公司、亳州金少堂中藥飲片有限公司、安國市盛輝中藥飲片有限公司、廣東美泰藥業(yè)有限公司、四川源上草中藥飲片有限公司、巫山縣醫(yī)藥公司中藥飲片廠等企業(yè)生產(chǎn)的8批次人參不合格。不合格項目為農(nóng)藥殘留。
對上述不合格中藥飲片,相關(guān)省級食品藥品監(jiān)督管理部門已采取查封、扣押等控制措施,要求企業(yè)暫停銷售和使用,召回產(chǎn)品,并進行整改。
要求中國食品藥品監(jiān)督管理局相關(guān)單位所在地省級食品藥品監(jiān)督管理部門依據(jù)《中華人民共和國藥品管理法》第七十三條、第七十四條、第七十五條對上述企業(yè)生產(chǎn)銷售不合格藥品的違法行為進行調(diào)查,并在三個月內(nèi)公開相關(guān)單位生產(chǎn)銷售不合格藥品的處理結(jié)果,及時報告相關(guān)情況。
在調(diào)查工作中,企業(yè)對產(chǎn)品真實性有異議的,可以向所在地省級食品藥品監(jiān)督管理部門提出,由省級食品藥品監(jiān)督管理部門對企業(yè)生產(chǎn)銷售情況進行調(diào)查核實,并告知被抽樣單位所在地省級食品藥品監(jiān)督管理部門。抽樣單位所在地省級食品藥品監(jiān)督管理部門收到不合格產(chǎn)品真實性異議通知后,應(yīng)當(dāng)立即立案調(diào)查,并追溯產(chǎn)品來源。確由有標(biāo)志的生產(chǎn)企業(yè)生產(chǎn)的,相關(guān)省級食品藥品監(jiān)督管理部門應(yīng)當(dāng)對生產(chǎn)企業(yè)從重處罰。