文|木易
CAR-T產品獲批在即,花落誰家撲朔迷離
從三強爭霸到兩虎相爭,CAR-T療法的競爭一直沒有走出過人們的視線,究竟哪家的產品會搶占先機,率先獲得FDA批準成為首個獲批的CAR-T療法,一直是人們時刻關注的話題。
2017年3月3日,諾華的CTL019(tisagenlecleucel-T)生物制劑獲得了美國FDA優先審評資格,其首款CAR-T生物制劑許可申請的審批流程有望得到進一步的縮減。這則消息的公布,又一次吊足了人們的胃口,令這場曠日持久的競爭結果又顯得撲朔迷離。
而就在不到1個月之前,Juno正式宣布放棄其CAR-T產品 JCAR015,轉而重點發展其管線中的其他CAR-T產品JCAR017及JCAR014。此時,距離Juno在臨床試驗中遭受又一次重大挫折已經過去了3個月的時間,其臨床試驗先后兩次因為導致患者的死亡而被FDA叫停。
去年4月,JUNO與國內藥明康德聯合成立上海藥明巨諾生物科技有限公司(JW Biotechnology Co. Ltd),雙方將結合Juno的CAR-T技術和T細胞受體技術,以及藥明康德的研發生產平臺及豐富的中國本地市場經驗,聯合打造中國領先的細胞療法公司,為血液腫瘤和實體腫瘤病人開發創新的細胞免疫療法。
除了諾華和Juno這兩家公司一家歡喜一家愁之外,Kite公司也是動作不斷,前不久也是剛公布了其CD28的CAR-TKTE-C19的亮眼臨床數據。
除此以外,今年1月10日,國內復星醫藥與全球領先的生物技術公司Kite Pharma聯合成立復星醫藥凱特生物科技(中國)有限公司,雙方各持合資公司50%的股權。合資公司將獲得KET-C19的中國商業化權利及后續兩個產品(KITE-439、KITE-718)授權許可的優先選擇權。
除以上三家采用自體移植方法的第一梯隊公司之外,不少其他公司也頗具競爭力,比如2017年3月份,Servier、Pfizer和Cellectis公司剛聯合宣布,美國FDA已經批準了通用型CAR-T療法UCART19用于治療復發/難治性急性淋巴細胞白血病患者的IND申請,隨后將在美國進入臨床開發;Bluebird與Celgene也開始了以B細胞成熟抗原(BCMA)為靶點的產品候選物的合作研發,并于2016年開始了臨床試驗,當年末也公布了I期臨床試驗的中期數據。
中國躋身全球CAR-T細胞治療研究第一梯隊
隨著CAR-T細胞治療在中國的研發快速發展,中國已然成為在CAR-T臨床研究項目上與美國同列為全球CAR-T研究的第一梯隊。據美國Clinical Trials.gov 網站對“Chimeric receptor”的搜索結果,截止目前中國登記開展CAR-T臨床研究項目90項,已經在數量上超過歐洲,僅次于美國。
前不久,藥明巨諾、吉凱基因、科濟生物、復星凱特、恒潤達生、東富龍、君實生物、天慈生物谷、嘉和生物9家公司發起召開上海細胞免疫治療技術聯盟成立預備會。接下來筆者將介紹國內5家涉及CAR-T細胞治療的公司。
科濟生物醫藥(上海)有限公司
科濟生物醫藥專注開展新型腫瘤免疫治療的探索與開發,成立于2014年10月30日,已開發出針對多種惡性實體腫瘤的嵌合抗原受體(CAR-T)細胞治療。秉承“科學創造,濟世救人”的理念,科濟生物醫藥已將全世界第一個針對肝細胞肝癌(HCC)以及針對多形性腦膠質瘤(GBM)推上臨床研究階段。
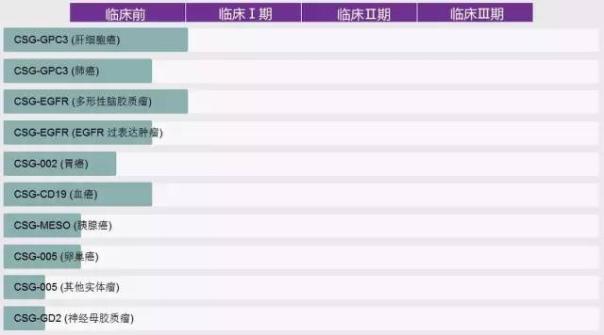
科濟生物醫藥候選產品管線
我們都知道CAR-T成功與否的關鍵就是作為GPS定位部件的抗體,科濟生物醫藥擁有一整套人源化抗體及全人抗體篩選平臺。從雜交瘤平臺和噬菌體文庫篩選得到的抗體通過進一步的優化來提高特性,如:抗體安全性、理化性質、功能特性及效力。
當然,對于CAR-T在實體瘤中遭遇的難點,主要是腫瘤組織的浸潤屏障與復雜的免疫微環境對CAR-T殺死癌細胞的影響,科濟生物醫藥通過結合諸如IL-12趨化因子受體或細胞因子彌合先天和適應性免疫增加對實體瘤的殺死療效。
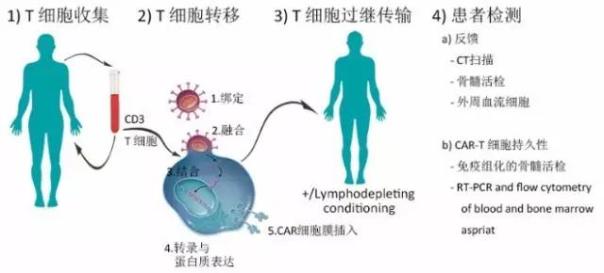
科濟生物醫藥的新一代CAR-T技術
創新技術、多管齊下的研發管線以及經驗豐富的創始團隊,使得科濟生物醫藥深受資本市場的青睞。2014年11月科濟生物醫藥完成A輪融資。2016年1月25日再次獲得3000萬美元的B輪融資,由韓國最早的風險投資公司KTB Ventures以及Jolly Innovation Ventures領投,Kaitai Capital和JIC Genesis Fountain Healthcare Ventures等參投。
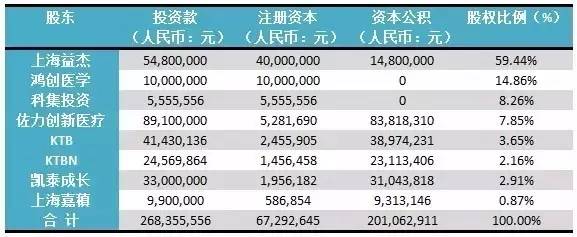
B輪增資后科濟生物醫藥的注冊資本及股權結構
上海恒潤達生生物科技有限公司
恒潤達生以腫瘤免疫治療技術研發為主業,同步轉化國內外最新的腫瘤免疫治療的進展。這家由頂級海歸和本土精英共同創辦的研發企業已經形成了CAR-T技術為主導,CAR-NK,新型DC疫苗和iNKT等多個研發項目并行推進的研發格局。
目前,恒潤達生已布局多項CAR-T細胞研發產品線,涉及適應癥主要在多發性骨髓瘤、成人及兒童B細胞白血病,B細胞淋巴瘤等。

恒潤達生的研發產品線及進度
2016年2月,恒潤達生在ClinicalTrial上成功注冊3個CAR-T治療B細胞淋巴瘤臨床試驗。其中,MatchCAR (NCT02685670)試驗已在國內臨床試驗基地入組復發難治性B細胞白血病患者共15例,11例回輸患者均達到完全緩解。MeCAR (NCT03652910)試驗也已在國內臨床試驗基地入組復發難治性B淋巴瘤患者10例,完成回輸的患者8例。

恒潤達生在ClinicalTrial上的3項臨床試驗
上海吉凱基因化學技術有限公司
吉凱基因成立于2002年,專注于疾病關鍵基因研究的綜合服務。準確來講,吉凱基因致力于轉化醫學,近年來將CAR-T細胞免疫治療作為重點發展戰略,以“CAR-T細胞免疫治療技術”的臨床轉化為目的,提供CAR-T細胞制備工具、臨床前體外細胞實驗、臨床前體內驗證實驗等服務,后期也為聯合申請臨床試驗提供技術支持。
吉凱基因的CAR-T技術平臺涵蓋了從一代CAR到四代CAR的構建技術,目前主要以臨床試驗效果最好的二代CAR結構為主,構建了從血液腫瘤到實體腫瘤多種不同的靶標scFv-CAR庫。

吉凱基因的研發管線
此外,吉凱基因已與長海醫院血液科合作開展CD19-CART治療復發難治B-ALL, CLL和B-NHL的臨床試驗研究,美國clinical trial注冊的臨床試驗號為:NCT02672501,已招募受試者14名,其中12例患者完全緩解至今無一例病人出現嚴重并發癥而死亡。
當然,吉凱基因同樣獲得資本資產的追捧,截至目前以完成兩輪融資,根據火石創造的Hsmap收錄顯示如下:

上海斯丹賽生物技術有限公司
斯丹賽由“國家杰出青年基金”獲得者肖磊博士創建于2009年8月,清晰定位CAR-T細胞治療領域,在細胞治療、干細胞和基因編輯等領域申報了30余項美國、中國、以及PCT發明專利。
截止2016年8月,斯丹賽在國內多家三甲醫院開展的多中心臨床試驗的26例入組急淋白血病患者中,有21例獲得完全緩解并達到微小疾病殘留陰性,完全緩解率為80.8%,病人6個月整體存活率為69.0%。
淋巴瘤方面,斯丹賽近期開展的兩例復發難治淋巴瘤臨床試驗的患者經過CAR-T治療也都取得了完全緩解。
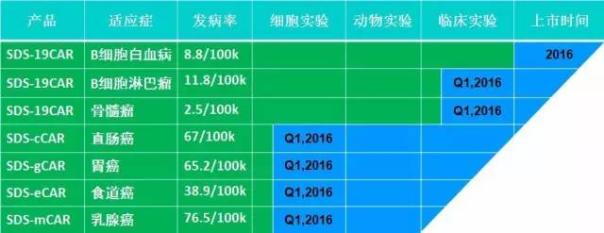
斯丹賽的研發管線
西比曼生物科技有限公司
西比曼成立于2009年,專注于打造多元化細胞治療技術平臺-腫瘤免疫細胞治療技術平臺和干細胞技術平臺,擁有美國AABB和ISO9001認證的cGMP研發與生產基地,擁有干細胞和免疫細胞技術國際專利10項、中國專利50余項。2014年在美國納斯達克掛牌上市。
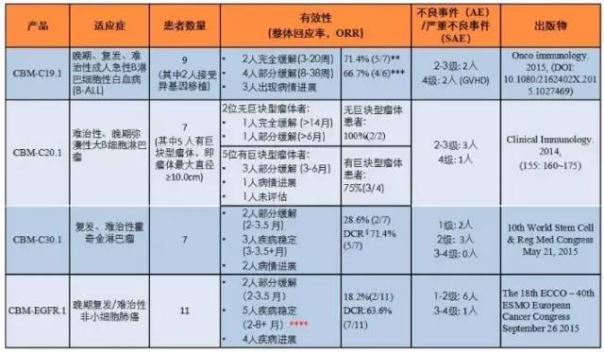
西比曼在CAR-T療法的臨床試驗主要集中在I/II期,涉及產品有:
CBM-C19.1:急性B淋巴細胞性白血病CBM-C20.1:非霍奇金淋巴瘤CBM-C30.1:霍奇金淋巴瘤CBM-EGFR.1:實體腫瘤
2015年上半年公司公布的I期臨床數據初步顯示相對安全、可行和有效。如下圖所示:
結語
作為新興的精準醫學治療手段,以CAR-T細胞治療為代表的免疫療法得到了快速發展,普遍被認為是人類最有希望攻克癌癥的創新療法之一。國外機構預測CAR-T細胞治療的市場空間也將超過1000億美元,國內情況亦是如此。
但是就比錢CAR-T而言,費用昂貴是一方面限制原因,適應癥限制也造成CAR-T技術無法取得突破性進展。如果其在實體瘤治療上取得突破性的進展,那么市場空間的非常值得我們想象。不過其實最重要的一點還是安全性問題,否則CAR-T技術的應用將僅僅是紙上談兵。