眾所周知,藥物進入體內(nèi)后,可以在各種酶的催化下發(fā)生代謝轉(zhuǎn)化,產(chǎn)生結(jié)構(gòu)相似的代謝產(chǎn)物。雖然結(jié)構(gòu)與母藥相似,但代謝物肯定是項目研發(fā)中的新化學成分。通過動物和體外方法對候選化合物進行毒理學研究,通常更關(guān)注母體藥物的特性,而不是代謝產(chǎn)物。而且動物物種和人體可能存在差異,不能簡單地假設產(chǎn)生的代謝產(chǎn)物和人體產(chǎn)生的是一樣的。當人體內(nèi)某些代謝產(chǎn)物的暴露量與動物種類不成比例時,就會存在安全風險。因此,提出了安全性檢測中代謝物的概念。
自20世紀90年代初以來,液相色譜-質(zhì)譜聯(lián)用技術(shù)(LC-MS)取得了突破性的發(fā)展,創(chuàng)新了藥物代謝領(lǐng)域的技術(shù)手段,使得在血漿等復雜底物中鑒定代謝物變得相對容易。再加上放射性標記的ADME(吸收、分布、代謝和排泄)研究,可以生成血漿、尿液和糞便的定量代謝物譜,使得代謝物研究成為藥物研發(fā)的重要組成部分。
雖然開發(fā)團隊都知道一般藥物的代謝物可能具有藥理活性或毒性作用,需要進行研究,但具體到項目,它們面臨以下問題:
1.哪些代謝物需要納入安全性評價范圍?
2.是否有代謝物暴露的閾值來確定進一步研究的必要性?
3.有必要獲取代謝物的化學結(jié)構(gòu)嗎?
這些都需要有相關(guān)的法律法規(guī)或者指導原則來遵循。
MIST指導原則的變遷
2002年,備受人體代謝物安全性困擾的行業(yè)率先“出擊”。來自不同公司和組織的一組科學家聯(lián)合發(fā)表了一份關(guān)于藥物代謝物風險評估的提案(參見第2條)。文章提出,在臨床前毒理學物種研究中,必須涵蓋人體血漿中暴露量占藥物相關(guān)物質(zhì)總量25%以上的代謝物。這是關(guān)于薄霧的第一次論述。
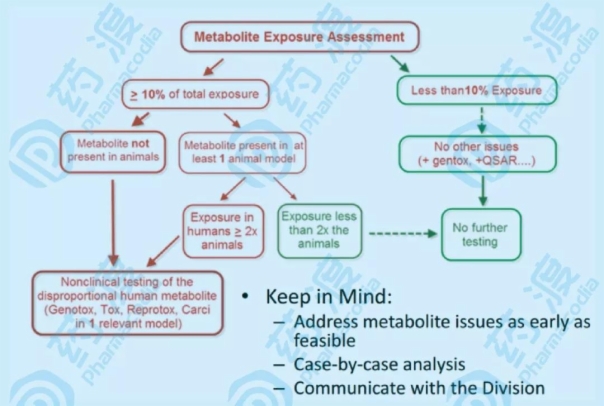
2008年,F(xiàn)DA終于發(fā)布了MIST的指導原則,將人體血漿中代謝物的閾值調(diào)整為藥物原型的10%。
2010年,ICH在綜合了更廣泛的意見后發(fā)布了指導意見,提出在進行大規(guī)模臨床試驗前,有必要對人體血漿中暴露量占藥物相關(guān)物質(zhì)總量10%以上的代謝物進行非臨床安全性研究(ICH M3(R2))。FDA隨后跟進并于2016年修訂了指南,以符合ICH。

毫無疑問,這些指導原則可以促進藥物安全性研究,但更重要的是,它們?yōu)樗幬镅邪l(fā)提供了一個研究代謝產(chǎn)物的框架。從臨床前到臨床,每個階段要解決的藥物代謝問題是不一樣的,可能會因策略和靶點的不同而不同。比如腫瘤晚期、耐藥HIV(艾滋病病毒)、先天性酶缺乏癥等嚴重疾病的藥物研發(fā)等。對代謝物的安全性研究有相應的簡化措施。對于常規(guī)項目,代謝物的典型策略可分為三個階段:
第一階段(前IND)
現(xiàn)階段藥物代謝研究主要集中在體外和體內(nèi)動物,如肝微粒體、肝細胞、肝S9、重組酶或血漿。將這些體外模型用于孵育代謝物,結(jié)合保留時間和質(zhì)譜裂解規(guī)律,比較不同物種與人類之間代謝物的定性/定量差異。在此基礎(chǔ)上,選擇合適的物種進行毒理學研究。或者研究給藥后動物的代謝產(chǎn)物,補充體外研究。動物的體內(nèi)結(jié)果不能直接轉(zhuǎn)化為準確的臨床預測,但通過分析動物的主要代謝產(chǎn)物,我們可以判斷代謝產(chǎn)物譜是否能覆蓋人類的結(jié)果,這對臨床安全性研究非常重要。
第二階段(臨床階段I)
來自臨床I期多劑量遞增試驗(MAD)的穩(wěn)態(tài)血漿樣本可用于人體代謝物的研究,這通常是首次獲得藥物的人體代謝物數(shù)據(jù)。雖然LC-MS的靈敏度可以滿足痕量代謝物的分析,但是合成代謝物標準品的工作量太大,而且代謝物的相對豐度
如何判斷《指導原則》中的代謝物是否超過藥物有關(guān)物質(zhì)總量的10%?如果將母藥和所有代謝物定量相加,需要大量的合成標準品,這顯然是不現(xiàn)實的。一般來說,在這個階段,不需要精確量化。只需將NOAEL(無明顯有害劑量)下的毒性種代謝物結(jié)果與臨床療效劑量下的血漿代謝物結(jié)果進行比較,即可確定是否存在臨床前未覆蓋的代謝物。常見的方法有兩種,一種是用漢密爾頓池法計算代謝物的“暴露倍數(shù)”;另一種是依靠同位素標記試驗,根據(jù)嚙齒動物同位素標記的物質(zhì)平衡結(jié)果,與大鼠同位素標記代謝物的濃度進行比較,得到因子,再換算成人代謝物的濃度。
一旦確定了臨床前代謝物的覆蓋范圍,就可以決定是否需要合成代謝物,是否需要進行專門的體內(nèi)和毒理學研究。但很多研究團隊選擇將這部分工作放回去,在完成人體同位素ADME的研究后再做決定,甚至將代謝物的研究放在臨床概念驗證(PoC)之后,也算是避免了因PoC的失敗而做過多的“無用功”。
第三階段(臨床階段II之后,臨床階段III之前)
因為主要代謝物的研究必須在臨床擴大前完成,所以所有必要的代謝物研究都應該在這個階段完成。包括代謝物的量化、通過高分辨率質(zhì)譜測定未知代謝物、研究人類同位素標記ADME(其也可用于確定哪些代謝物需要DDI評估)以獲得所有代謝物的光譜等。
對MIST的一些思考
自2008年FDA發(fā)布MIST指南至今已有十余年。在這十年間,代謝物和代謝安全的重要性逐漸深入人心。制藥行業(yè)已經(jīng)適應了MIST指南的要求,大量的案例也為R&D團隊的代謝物研究計劃提供了很好的參考。然而,遇到了許多問題。首先,很少有項目真正對代謝物進行毒理學研究,也很難找到循環(huán)代謝物直接導致安全問題的案例。很多情況下,明明安全性問題已經(jīng)指向了代謝物,但最后卻沒有完整的證據(jù)。一方面,這可能是由于難以區(qū)分代謝物與母體藥物的性質(zhì);另一方面,對于一些活性中間代謝物,常規(guī)分析方法有時無法檢測出來,造成很大困難。大鼠服用恩格列吡嗪后,觀察到明顯的代謝產(chǎn)物介導的毒性,但未發(fā)現(xiàn)活性代謝產(chǎn)物和下游代謝產(chǎn)物。
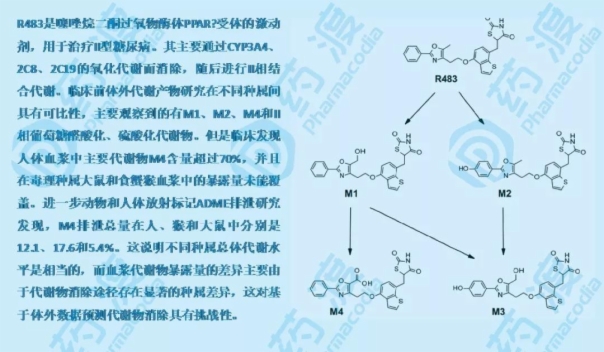
其次,反應性代謝產(chǎn)物或下游產(chǎn)物(如谷胱甘肽或半胱氨酸結(jié)合物的代謝產(chǎn)物)由于分子量大、親水性強,通常通過膽汁和/或尿液快速排泄,因此很難根據(jù)MIST的要求比較不同物種間反應性代謝產(chǎn)物的暴露差異。此外,在一些特定項目中,目標組織中代謝物的測定可能更重要,但在人體中很難進行。換句話說,隨著技術(shù)的發(fā)展,對代謝物的研究應該做到什么程度?MIST所做的一切是否真的影響了藥物安全性的評價,是我們今后需要思考和解決的問題。

指導原則只是提供了一個方向。對于每一個項目,都需要設計一個具體情況具體分析的研究方案。除了常規(guī)毒性外,我們還應注意代謝物潛在的DDI發(fā)生。吉非羅齊的葡萄糖醛酸化代謝產(chǎn)物抑制西立伐他汀的代謝清除(主要由CYP2C8和OATP1B1介導),導致嚴重后果。此外,還有丁苯丙酮的代謝產(chǎn)物對CYP2D6表達水平的影響,以及去甲基地爾硫卓對CYP3A4的抑制作用。FDA和EMA的指南建議,當代謝物的體內(nèi)水平達到母體藥物的25%(FDA,2012)或暴露量超過藥物總暴露量的10%(EMA,2012)時,需要研究代謝物的CYP抑制和轉(zhuǎn)運體抑制。在2017年FDA新指導原則草案中,進一步要求對警示化學結(jié)構(gòu)(官能團)進行TDI(時間依賴性抑制)研究;對于極性小于母體藥物且暴露量大于母體藥物25%的代謝物,以及極性大于母體藥物且暴露量大于母體藥物的代謝物,需要進行體外DDI的研究。
總之,MIST指導原則的引入不僅是DMPK科學家的研究參考,而且在很大程度上也是藥學和藥理學科學家對代謝物安全性的足夠重視。只有這樣,新藥的安全性評價才能更加徹底,這也是MIST對藥物研發(fā)的最大貢獻。
參考文章:
[1]迷霧中的十年:從“安全性試驗中的代謝物”監(jiān)管指導下的藥物開發(fā)中的藥物代謝物研究中獲得的經(jīng)驗。DOI:
[2]安全性試驗中的藥物代謝物。DOI:10.1006/
[3]安全性試驗中的代謝物。
[4]FDA-工業(yè)用藥物代謝物安全性測試指南。
[5]M3工業(yè)部(R2)關(guān)于進行人體臨床試驗和藥品上市許可的非臨床安全性研究的指南。
[6]安全性試驗中的代謝物:臨床藥理學家的“迷霧”。doi:10.1038/