11月8日,百時美施貴寶(BMS)宣布,Nivolumab聯合化療作為IIIA非小細胞肺癌(NSCLC)可切除早期IB的新輔助治療的III期CheckMate-816研究已達到改善無事件生存率(EFS)的主要終點。
此前,CheckMate -816研究的pCR數據和手術結果發表在美國癌癥研究協會(AACR)2021年年會和美國臨床腫瘤學會(ASCO)2021年年會上。到目前為止,CheckMate-816是第一個針對NSCLC的新輔助免疫治療的III期試驗,以顯著提高無事件生存率(EFS)和完全病理反應(pCR)。
第一個吃螃蟹的人,并不好當
有理由相信,隨著CheckMate-816數據的成熟,Nivolumab可能在不久的將來獲得早期NSCLC的首個免疫治療方案。在基于IMpower010的atilizumab研究于近日被FDA批準用于早期NSCLC的輔助治療后,免疫治療在NSCLC中的應用有望繼續向前邁進,為肺癌患者帶來更多的長期生存希望。
然而,要成為第一個吃螃蟹的人,并不容易。不禁想起了第一個獲批的高危早期三陰性乳腺癌免疫治療方案的曲折歷程。
雖然領域不同,但另一個類似CheckMate-816的隨機雙盲III期試驗是著名的KEYNOTE-522 (NCT03036488)。本研究旨在評價帕博利珠單抗聯合化療在高危早期三陰性乳腺癌(TNBC)患者術前新輔助治療中的療效和安全性,并在術后繼續單一藥物作為輔助治療。常見的終點是pCR和EFS。從2017年5月開始臨床試驗,到2021年7月正式獲批,歷時四年。
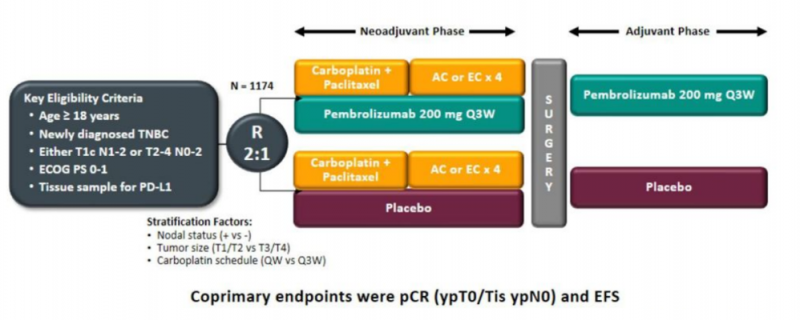
KEYNOTE-522研究設計
早在2019年歐洲醫學腫瘤學會(ESMO)會議上,KEYNOTE-522研究的pCR分析數據就已發表,隨后發表在《新英格蘭醫學雜志》上。根據pCR數據和EFS中期研究結果,莫東向FDA提交了Keytruda治療早期TNBC高危患者的補充生物制劑(sBLA)許可申請。然而,2021年3月,默沙東收到了FDA的完整回復,FDA的腫瘤藥物咨詢委員會(ODAC)在獲得KEYNOTE-522研究的成熟數據后,以10: 0的投票結果決定是否批準這一適應癥。
直到今年5月,默克公司宣布KEYNOTE-522研究已經達到EFS的第二個主要終點。兩個月后,FDA正式批準pabolizumab聯合化療用于高危早期三陰性乳腺癌的新輔助治療,術后繼續使用pabolizumab作為輔助治療。
在做出決定之前等待成熟數據的關鍵因素之一在于對替代終點pCR反映生存益處的普遍懷疑。可以想象,CheckMate-816也要面對這種詰問。
由于歷史發展的各種原因,在新輔助治療的臨床研究中有許多替代終點:EFS、pCR、MPR。它們到底是什么意思?它是如何演變的?為什么pCR陽性后還要等EFS結果被監管機構認可?接下來,我們來了解一下。
臨床研究也為“KPI指標”而煩惱
為了充分理解各種派生指標,我們需要首先澄清一個問題:什么是新援助?
一般來說,新輔助治療是術前的抗腫瘤治療,其次是手術切除。相應的,輔助治療是指手術后給予的治療。術前新輔助治療的主要優勢是降低術前腫瘤負荷,清除血液中的腫瘤細胞,達到減少術后復發轉移的目的,進而改善患者的預后。此外,新輔助治療后手術標本的病理緩解率可能成為術后生存的預測指標,可以指導復發高危人群及時進行輔助治療。
其中,基于死亡事件判斷的OS是反映生存獲益的“金標準”,非常穩健,不受研究者主觀因素的影響,但需要較長的隨訪時間和較大的樣本量。尤其是圍手術期治療,長期生存數據通常需要10年左右才能完成,這不僅成倍增加了研究成本,也使得交叉和后線治療的影響不可估量。
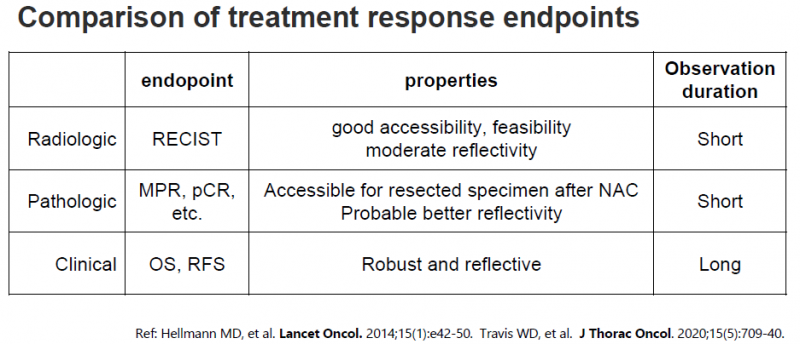
因此,對于治療反應的評價,通常采用基于影像學的實體瘤療效臨床評價標準(RECIST)來判斷疾病進展,如單臂臨床試驗中常用的客觀反應率(ORR)。另一個眾所周知的無進展生存期(PFS)結合了影像學評估和臨床評估,定義為從隨機分組到出現客觀腫瘤進展或全因死亡的時間。這是隨機對照臨床試驗中最常用的替代終點。
與PFS(無進展生存期)類似,還有DFS(無病生存期)和EFS(無事件生存期)。三者首字母與單詞的區別對應不同疾病階段的主要治療目標(KPI):3354轉移性疾病“無進展”(不繼續發展延長生存時間)、術后輔助/新輔助治療“無進展”
換句話說,EFS和PFS最大的區別是PFS觀察疾病進展/死亡事件;EFS觀察了疾病的復發/死亡,還包括了新佐劑的獨特終點事件:疾病進展未能起作用。
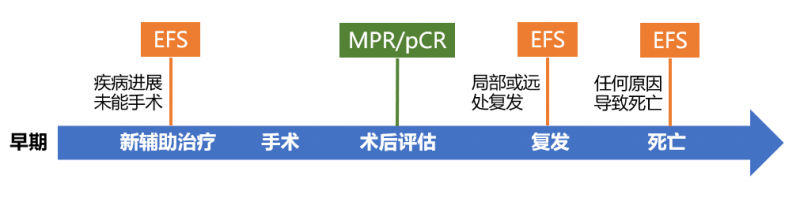
但對于新輔助免疫治療,由于影像學上存在“偽進展”現象(注:RECIST評分部分病例為進展或穩定,部分甚至完全緩解由病理評估),近年來越來越重視病理評估(pCR、MPR)。

病理完全緩解(pCR)到底是什么?
顧名思義,假定早期腫瘤患者在手術前接受新輔助治療后出現所謂的“治愈”。pCR被定義為在已經被清除的原發性腫瘤或淋巴結中沒有殘留的存活腫瘤細胞。
但是,又發現了新的問題。NSCLC新輔助化療的pCR極低,可能不適合作為替代指標。然后在2014年,Matthew Hellman教授提出了一個全新的——大病理緩解(MPR)的指標,定義為術后標本病理檢查殘留腫瘤細胞<10%。但是MPR只關注原發病灶,不關注淋巴結,需要更多的數據來證明臨界值。也有專家質疑MPR的判斷容易受主觀因素影響。相比之下,pCR可能是一個更可靠的終點,具有更大的室間一致性。
理想很豐滿,現實卻很骨感。對于非小細胞肺癌新輔助治療后的手術標本,目前缺乏完整可行的從大體到微觀的評估方法。2020年5月,國際肺癌研究協會(IASLC)發布的《新輔助治療后肺癌手術標本病理評估》多學科推薦方法成為重要參考標準。今年9月,國家癌癥質控中心肺癌質控專家委員會發布的《非小細胞肺癌新輔助治療療效病理評估專家共識》也標志著國內病理反應評價體系的進一步完善。
根據共識,在合理識別瘤床(注:瘤床是指治療前原發腫瘤所在的部位,新輔助治療后可能難以識別瘤床)、標本固定、標準化取樣后,可確定完全病理緩解(pCR)或顯著病理緩解(MPR)。共識建議將10%作為MPR的臨界值,并指出與普通標本相比,新輔助病理標本的評價過程較為復雜,準確性和一致性有待進一步提高。
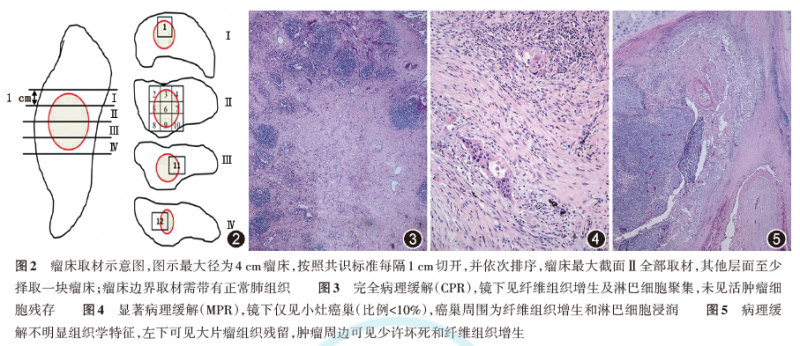
目前,對于早期高危乳腺癌,EFS和pCR已被FDA作為加速審批的替代終點,仍存在諸多爭議和質疑。在肺癌領域,EFS、pCR、MPR尚未寫入監管機構的指導性文件。哪個指數更好還是未知數。
回到之前的問題,無論是CheckMate-816還是KEYNOTE-522研究,為什么pCR陽性后還要等EFS結果?或許可以理解為,病理評估過程復雜,易受主觀因素影響,其穩健性、可重復性、室間一致性以及與長期效益的關系仍存在諸多不確定性。目前,綜合評價pCR和EFS這兩個常見主要終點的益處,更容易被監管機構所接受。
挑戰標準新輔助化療,還有幾道坎?
目前,免疫療法已逐漸成熟
人們對此充滿期待,因為從機制上來說,PD-1/PD-L1抑制劑需要腫瘤細胞提呈抗原才能殺死腫瘤,而當腫瘤體積較大時,抗原提呈細胞承受的抗原負荷更大,從而表現出更強的抗腫瘤T細胞反應。因此,新輔助免疫療法在理論上優于輔助免疫療法,患者可以獲得更大的生存獲益。幾項臨床前研究的發現也證實了上述觀點。
毫無疑問,任何一種治療方法都想從晚期走向早期,目的是成為標準治療。那么,圍手術期IO想要挑戰標準治療還有多少坎呢?
1.安全性:新輔助免疫治療后的手術安全性是外科醫生關注的焦點,但沒有客觀的評價指標。根據現有資料,新輔助免疫單藥和聯合化療并未導致大量延期手術。總體平均手術切除率為88.70%,沒有增加手術難度和圍手術期風險。手術并發癥的平均發生率為20.6%,大部分預后良好。基本上,死亡與藥物治療無關。
目前在小樣本研究中似乎安全性基本令人滿意,但免疫相關肺炎、心臟毒性、消化道毒性等罕見但嚴重的毒性仍值得臨床醫生高度重視。對此,今年3月發表在《中國肺癌雜志》上的《非小細胞肺癌圍手術期免疫治療相關不良反應管理的臨床診療建議》進行了較為詳細的闡述。
2.有效性:縱觀目前已達到主要研究終點的新輔助治療研究,總的趨勢是IO單藥或IO聯合化療,而免疫兩藥聯合表現不佳。
免疫單一療法的新輔助研究,如MATE159、LCMC3、PRINCEPS、TOPlS01、IoNESCO和ChicTR-OIC-17013726,被納入I -IIIb期NSCLC患者,在一到三個治療周期后,MPR在14%到45%之間。Ib -IIIa期患者入選聯合化療新輔助研究(NADIM,NCT02716038,SAKK 16/14),治療2 ~4個周期。NADIM研究的MPR率高達85.36%,pCR率為71.4%,其他兩項研究的MPR約為60%。雙重新輔助研究(NEOSTAR)包括I -IIIa期肺癌患者,治療3個周期,MPR率為24%。CheckMate 816是目前第一個達到主要終點的III期研究,我們期待更多詳細數據的發表。
3.病理評估終點和長期獲益之間的相關性:隨著更多的試驗使用MPR和pCR作為新輔助治療臨床獲益的替代指標,迫切需要清楚地證明這些病理評估終點反映生存獲益的程度。
一項回顧性分析顯示,新輔助化療后獲得MPR的患者的DFS和OS明顯長于未獲得MPR的患者。那么,這種效果適用于免疫聯合治療嗎?目前,大多數證據來自II期研究的事后分析。
在NADIM研究(Nivolumab化療)的后分析中,獲得MPR或pCR的患者的24個月OS率為100%,而病理反應不完全的患者的OS率為85.7%(P=0.002)。在另一項新的輔助免疫治療(atilizumab化療)臨床試驗中,事后分析顯示,有MPR和無MPR患者的中位DFS分別為34.5個月和14.3個月(P=0.71)。pCR、MPR與OS的關系仍需大量臨床資料驗證,MPR的定義需要更細致的探索和規范。
小結
還是有一些想法的。如何看待早期患者如此高的病理緩解率?接受新輔助IO后達到pCR可以“避免”手術嗎?在聯合化療的療程設計方面,是同時聯合化療,還是同療程后免疫治療,還是幾個療程后序貫免疫治療?應該減少劑量還是維持常規劑量?新輔助治療與手術間隔多長時間,并發癥最低?臨床上應該如何選擇患者?有正向驅動基因的患者需要選擇嗎?如何根據生物標志物篩選真正受益的人?
今年1月,《非小細胞肺癌新輔助免疫治療國際專家共識》發表在《轉化型肺癌研究》(《肺癌轉化研究》)雜志上。40多名專家就9種臨床治療方案達成一致。但是臨床上還是有太多的爭議和未知。在…里
相對于晚期腫瘤,圍手術期治療的研究時間跨度長,治療期間變化大,往往“十年磨一劍”。在漫長的研究期間,許多因素如治療藥物、治療策略、人群分布等。可能有較大變化,影響研究進度和結果。只有“耐得住寂寞”,才能做“忠實的妻子”。
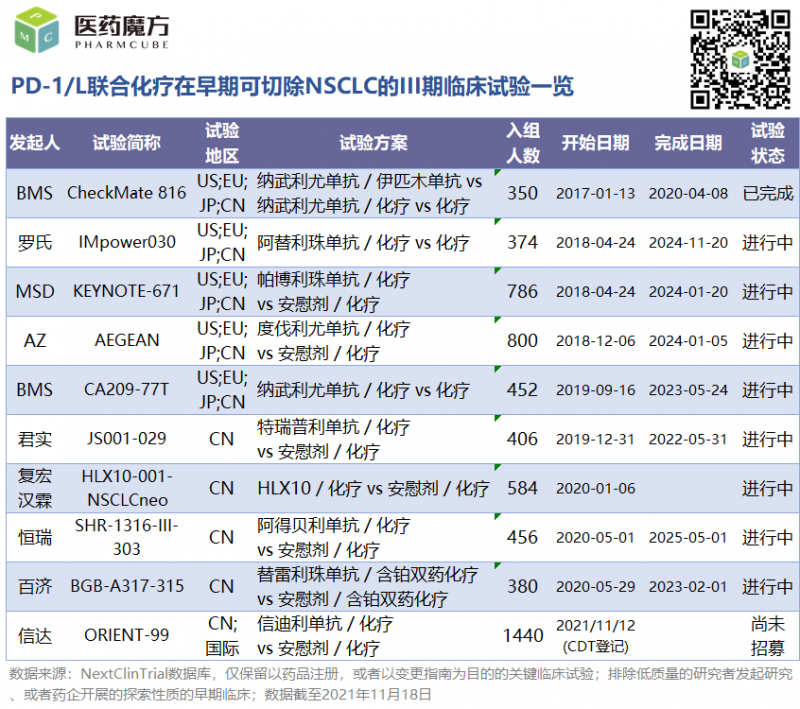
繼CheckMate816、IMpower030、KEYNOTE-671的研究之后,君實、百濟、恒瑞、傅宏翰林等國內企業也開始布局。信達近期開展了辛地利珠單抗聯合化療用于非小細胞肺癌術前新輔助和術后輔助治療的國際多中心III期研究(國內640人,全球800人)。我們有信心,這些臨床試驗將帶來更豐富的結果,解決圍手術期免疫治療的許多突出問題。
參考資料:
1.MPR和pCR作為新輔助WCLC治療的主要終點:(教育會議)
2.病理學完全緩解作為肺癌新輔助治療后的替代終點。柳葉刀腫瘤。2021年8月;22(8):1056-1058.
3.Neo是什么?可切除非小細胞肺癌的新輔助化療。臨床9月10日;39(26):2855-2858.
4.新輔助治療后肺癌切除標本病理評估的IASLC多學科建議。胸腔腫瘤學雜志。2020年5月;15(5):709-740.
5.非小細胞肺癌新輔助治療病理學評價專家共識[J].中華病理學雜志,2021,50(09):1002-1007。
6.非小細胞肺癌圍手術期免疫治療相關不良反應的臨床診治建議[J].中國肺癌雜志,2021,24(3):20。
7.2019中國肺癌高峰論壇訪談[J]。循證醫學,2019,(04):14-23。
8.非小細胞肺癌新輔助免疫治療專家共識。肺癌研究第2020號決議;9(6):2696-2715.
9.中國非小細胞肺癌免疫抑制治療專家共識(2020年版)[J].中國肺癌雜志,2021,24(4):19。
10.
